McKaizer Institute · Longevity & Wellness
The definitive guide to reversing cellular aging through senolytics, NAD+ restoration, and sirtuin activation. Harvard, Mayo Clinic, and Stanford protocols explained clearly.
50%
drop in cellular NAD+ between age 20 and 50 — the energy crisis at the heart of aging
Table of Contents
- The Day Scientists Proved Aging Was Optional
- Senescent Cells: The Zombie Crisis Within You
- Senolytics: The Science of Killing Zombie Cells
- NAD+: Your Cells’ Master Energy Molecule Is Running Out
- Sirtuins: The Longevity Genes That NAD+ Wakes Up
- The Complete Cellular Rejuvenation Protocol
- Measuring Your Biological Age: The Biomarker System
- The 250-Year Horizon: What Partial Reprogramming Changes Everything
- Frequently Asked Questions
- References & Citations
The Day Scientists Proved Aging Was Optional
She was 67 on her driver’s license. But the epigenetic clock said something else entirely.
After 14 months of targeted intervention — senolytics, NAD+ restoration, and precision nutrition — Dr. Kara Fitzgerald’s patient tested at a biological age of 54. Thirteen years younger. Not cosmetically. Cellularly.
This wasn’t science fiction. It was a peer-reviewed study published in Aging (2021). And it was only possible because of a discovery made a decade earlier — in a mouse lab at the Mayo Clinic — that shattered everything we thought we knew about growing old.
The Experiment That Rewrote Biology
In 2011, cell biologist Jan van Deursen wasn’t trying to reverse aging. He was studying cancer.
His team at the Mayo Clinic had engineered a strain of mice carrying a genetic switch. When activated, it would selectively destroy senescent cells — damaged, dysfunctional cells that refuse to die. Cells that accumulate in your tissues as you age. Cells that scientists would soon call “zombie cells.”
What happened next changed the trajectory of modern medicine.
When van Deursen’s team cleared senescent cells from prematurely aging mice, the animals didn’t just slow down their decline. They got younger:
- Cataracts reversed
- Muscle loss stopped — and rebuilt
- Fat tissue dysfunction disappeared
- Kidney and heart function improved dramatically
- The mice lived 25-35% longer than untreated controls
The paper landed in Nature like a thunderclap. It proved, for the first time in history, that aging was not merely a passive process of wear and tear. It was actively driven by identifiable cellular mechanisms — and those mechanisms could be interrupted.
💡 Quick Fact: By age 60, an estimated 30-70% of cells in some tissues are senescent — silently secreting inflammatory molecules that damage everything around them.
What This Means For You
You are not simply “getting older.” Your body is accumulating zombie cells that poison healthy tissue. The revolutionary insight from van Deursen’s lab is this: remove the poison, and the body begins to heal itself. This is no longer theoretical. It is the foundation of an entirely new medical paradigm.
The Three Pillars of the New Longevity Science
Van Deursen’s discovery didn’t exist in isolation. It converged with two other breakthroughs that, together, form the three pillars of modern age-reversal science.
Pillar 1: Senolytics — Clearing the Zombie Cells
Senolytics are compounds that selectively eliminate senescent cells. The most studied combination — dasatinib + quercetin (D+Q) — was shown by the Mayo Clinic’s Dr. James Kirkland to:
- Reduce senescent cell burden in humans within 3 days of treatment
- Improve physical function in patients with idiopathic pulmonary fibrosis
- Decrease inflammatory markers tied to cardiovascular disease, diabetes, and neurodegeneration
Human trials are now underway at over a dozen major research institutions worldwide.
Pillar 2: NAD+ Restoration — Refueling Cellular Energy
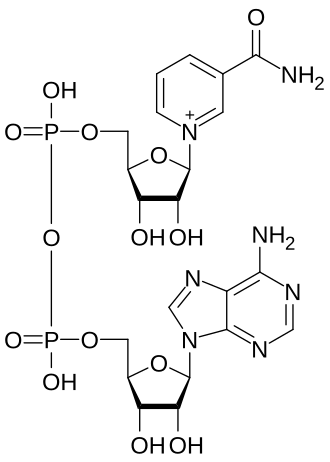
Nicotinamide adenine dinucleotide (NAD+) is a coenzyme present in every living cell. It is essential for DNA repair, mitochondrial function, and energy metabolism. And it declines 50% or more between ages 40 and 60.
Harvard geneticist David Sinclair demonstrated that restoring NAD+ levels via precursors like NMN (nicotinamide mononucleotide) could:
- Reverse vascular aging in mice, making old blood vessels indistinguishable from young ones
- Restore muscle function and exercise capacity in aged animals
- Improve DNA repair efficiency by activating key repair enzymes
Pillar 3: Sirtuins — The Master Regulators
Sirtuins are a family of seven proteins that regulate everything from inflammation to metabolism to chromosomal stability. Think of them as your body’s cellular maintenance crew. They require NAD+ to function — which is why NAD+ decline creates a devastating cascade.
When sirtuins are active, your cells:
- Silence damaged genes before they cause problems
- Boost mitochondrial output for sustained energy
- Reduce chronic inflammation at the molecular level
- Enhance stress resilience across every organ system
💡 Quick Fact: Caloric restriction — the oldest known longevity intervention — works largely because it activates sirtuins. Fasting mimetics aim to trigger the same pathways without the hunger.
The Hallmarks of Aging: A Unified Framework
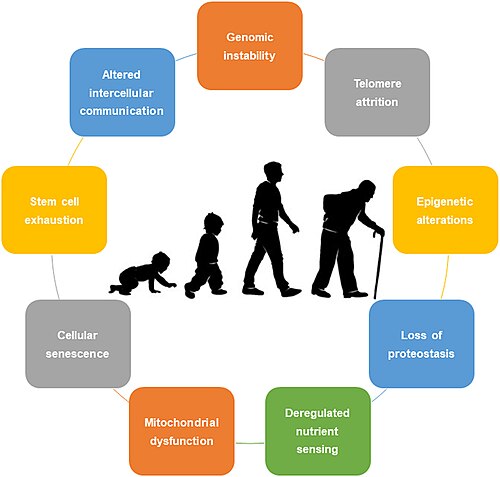
In 2013, researchers Carlos López-Otín, Maria Blasco, Linda Partridge, Manuel Serrano, and Guido Kroemer published a landmark paper in Cell that organized the chaos. They identified nine — now updated to twelve — Hallmarks of Aging:
- Genomic instability
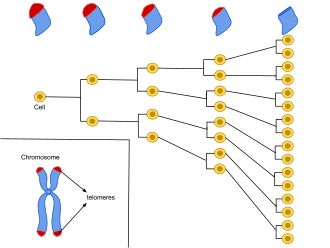
- Telomere attrition
- Epigenetic alterations
- Loss of proteostasis
- Disabled macroautophagy
- Deregulated nutrient-sensing
- Mitochondrial dysfunction
- Cellular senescence
- Stem cell exhaustion
- Altered intercellular communication
- Chronic inflammation
- Dysbiosis
This framework gave the field a shared language. Every intervention — from senolytics to NAD+ boosters to rapamycin — could now be mapped to specific hallmarks. Aging was no longer a vague mystery. It was an engineering problem with defined targets.
What This Means For You
You do not need to wait for a single miracle drug. The hallmarks framework reveals that aging is multi-causal — and the most powerful strategies address multiple hallmarks simultaneously. Nutrition, movement, sleep, and targeted supplementation can hit six or more hallmarks at once.
The question is no longer can aging be slowed. It’s how aggressively are you willing to act on what science already knows.
Key Points
- Jan van Deursen’s 2011 Mayo Clinic experiment proved that clearing senescent cells can reverse age-related decline and extend lifespan by 25-35% in mice
- Three converging breakthroughs — senolytics, NAD+ restoration, and sirtuin activation — form the foundation of modern longevity science
- The Hallmarks of Aging framework transformed aging from an unsolvable mystery into a targetable, multi-pathway engineering problem — and you can start addressing it today
Senescent Cells: The Zombie Crisis Within You
They don’t die. They don’t divide. And they won’t leave quietly.
Senescent cells are former healthy cells that have suffered irreparable damage — from DNA breaks, telomere erosion, oxidative stress, or oncogenic signals. Instead of doing what damaged cells are supposed to do (self-destruct through apoptosis), they enter a state of permanent arrest. They stop functioning. But they refuse to die.
And that refusal is slowly poisoning you from the inside out.
The Biology of a Zombie Cell
Under normal circumstances, cellular senescence is actually a protective mechanism. When a cell’s DNA is too damaged to safely replicate, senescence acts as an emergency brake — halting division to prevent that cell from becoming cancerous.
In youth, your immune system efficiently identifies and clears these arrested cells. Natural killer (NK) cells and macrophages patrol your tissues, tagging senescent cells for removal and disposing of them within days.
The system works beautifully — when you’re 25.
But as immune function declines with age — a process called immunosenescence — clearance slows. Senescent cells begin to accumulate. They embed themselves in your tissues like squatters who refuse eviction. And then they start doing something far worse than simply taking up space.
They start talking.
The SASP: A Toxic Broadcast Signal
In 1999, cell biologist Judith Campisi at the Buck Institute for Research on Aging made a discovery that would reshape our understanding of how we deteriorate.
She identified that senescent cells don’t sit quietly. They actively secrete a devastating cocktail of inflammatory molecules — a phenomenon she named the Senescence-Associated Secretory Phenotype, or SASP.
💡 Quick Fact: A single senescent cell can secrete over 40 different pro-inflammatory cytokines, chemokines, growth factors, and proteases — continuously, for years.
The SASP includes some of the most destructive molecules in human biology:
- IL-6 and IL-1β — master inflammatory cytokines that drive systemic chronic inflammation
- TNF-α — a tumor necrosis factor linked to insulin resistance, muscle wasting, and neurodegeneration
- MMP-3 and MMP-9 — matrix metalloproteinases that physically degrade the structural tissue around the senescent cell
- VEGF — a growth factor that promotes abnormal blood vessel formation, fueling tumor growth
- MCP-1 — a chemokine that recruits immune cells, amplifying local inflammation into a tissue-wide crisis
Here’s what makes this truly dangerous. The SASP doesn’t just damage surrounding tissue. It converts neighboring healthy cells into senescent cells.
Campisi’s research demonstrated this bystander effect — a single zombie cell can trigger a cascade of senescence in the cells around it. One becomes ten. Ten becomes hundreds. It’s a biological contagion operating inside your own body.
What This Means For You
Every senescent cell in your body is a tiny inflammation factory running 24 hours a day, 7 days a week. The SASP is now recognized as one of the primary drivers of inflammaging — the chronic, low-grade inflammation that underpins virtually every age-related disease. Silencing or clearing these cells doesn’t just slow aging. It removes one of its root causes.
The Accumulation Curve: From 2% to 15%
In your twenties and thirties, senescent cells comprise roughly 1-2% of your total cell population. Your immune system keeps pace. Damage is repaired or removed. Tissue function remains high.
By your forties, clearance begins falling behind. Senescent cell burden climbs to 4-6%. You may not feel it yet — but inflammatory markers are rising, tissue repair is slowing, and organ reserve is quietly diminishing.
By age 60-70, senescent cells can represent 10-15% of the cells in affected tissues. At this concentration, the SASP output reaches a tipping point. Tissue architecture begins to visibly and functionally collapse.
The organs hit hardest are the ones you can least afford to lose:
- Skin — senescent fibroblasts degrade collagen and elastin, driving wrinkles, thinning, and impaired wound healing
- Kidneys — senescent tubular cells accelerate nephron loss; kidney function can decline 30-40% by age 70
- Lungs — senescent alveolar cells reduce gas exchange efficiency and drive pulmonary fibrosis
- Liver — senescent hepatocytes impair detoxification, lipid metabolism, and regenerative capacity
- Joints — senescent chondrocytes in cartilage are a primary driver of osteoarthritis, degrading the tissue from within
- Vasculature — senescent endothelial cells stiffen arteries, promote plaque formation, and elevate cardiovascular risk
- Brain — senescent astrocytes and microglia amplify neuroinflammation, now linked to Alzheimer’s, Parkinson’s, and cognitive decline
💡 Quick Fact: In a landmark 2018 study published in Nature Medicine, researchers at Mayo Clinic showed that transplanting just a small number of senescent cells into young mice caused persistent physical dysfunction, reduced survival, and accelerated biological aging — proving that senescent cells alone are sufficient to cause aging phenotypes.
Measuring Your Senescent Burden
You can’t manage what you can’t measure. Until recently, quantifying senescent cell load required tissue biopsies — impractical for routine monitoring. That’s changing rapidly.
Current and emerging measurement approaches include:
- p16^INK4a expression (blood-based) — p16 is the most validated biomarker of cellular senescence; rising levels in circulating T cells correlate strongly with biological age and senescent burden
- High-sensitivity C-reactive protein (hsCRP) — while not specific to senescence, elevated hsCRP reflects the systemic inflammatory output of SASP; optimal is below 0.5 mg/L, yet most adults over 50 measure 2.0-4.0 mg/L
- IL-6 and TNF-α panels — direct measurement of key SASP cytokines; these advanced inflammatory panels are available through functional medicine labs
- GlycanAge testing — measures glycan patterns on immunoglobulin G that shift with inflammatory and senescent burden, providing a proxy for immune aging
- SA-β-galactosidase activity — the gold standard in research settings; detects senescence-associated enzyme activity in tissue samples
- Epigenetic clocks (GrimAge, DunedinPACE) — while not senescence-specific, these clocks capture the downstream biological aging driven by senescent cell accumulation and SASP exposure
What This Means For You
You don’t need a research lab to start tracking this. A combination of hsCRP, IL-6, and an epigenetic clock test gives you a practical, actionable picture of your inflammatory and senescent burden today. Test annually. Track your trajectory. The goal isn’t a single number — it’s a declining trend over time as you implement clearance strategies.
Key Points
- Senescent cells are damaged cells that refuse to die, accumulating from ~2% of cells in your 20s to 10-15% by age 70 — and they actively poison surrounding tissue through the SASP
- Judith Campisi’s discovery of the Senescence-Associated Secretory Phenotype revealed that each zombie cell secretes 40+ inflammatory molecules, converting healthy neighbors into senescent cells and driving organ-level decline in the brain, kidneys, lungs, joints, and vasculature
- Measurable today through a combination of hsCRP, IL-6 panels, p16^INK4a expression, and epigenetic clocks — giving you a practical baseline to track and reduce your senescent burden year over year
“Aging is not simply time passing. It is the loss of epigenetic information. And what has been lost can, at least in part, be restored.”
Senolytics: The Science of Killing Zombie Cells
For decades, medicine had no answer to cellular senescence. We could slow it. We could measure it. But we couldn’t selectively eliminate the cells driving it.
That changed in 2015. And it may be the most important breakthrough in longevity science this century.
Senolytics are a new class of compounds designed to do one thing: find senescent cells and kill them — while leaving healthy cells untouched. Not slowing aging. Not managing symptoms. Removing the source.
The field has moved from petri dishes to human trials in under a decade. Here’s where the science stands right now.
The Breakthrough: Dasatinib + Quercetin (D+Q)
The story begins at the Mayo Clinic with Drs. James Kirkland and Tamara Tchkonia.
Their insight was elegant. Senescent cells survive because they upregulate anti-apoptotic pathways — essentially, molecular shields that prevent them from undergoing programmed cell death. They’re damaged beyond repair, but they’ve hacked their own self-destruct mechanism.
Kirkland’s team asked a simple question: what if we disable the shields?
They screened dozens of compounds and found a powerful combination:
- Dasatinib — a cancer drug that inhibits tyrosine kinases and ephrin receptor signaling, targeting senescent fat cell progenitors and vasculature
- Quercetin — a plant flavonoid that inhibits BCL-2 family proteins, PI3K, and serpine, targeting senescent endothelial cells and bone marrow stem cells
Alone, each compound was moderately effective. Together, they were devastating — clearing senescent cells across multiple tissue types simultaneously.
💡 Quick Fact: In Kirkland’s landmark 2019 mouse study, a single round of D+Q extended remaining lifespan by 36% in aged mice — equivalent to adding roughly 9 human years from a single treatment window.
From Mice to Humans
The Mayo team moved fast. Their key human results:
- 2019 pilot trial in patients with idiopathic pulmonary fibrosis (a disease driven by senescent cell accumulation): just 3 doses over 3 weeks produced measurable improvements in 6-minute walk distance, chair-stand speed, and SASP biomarker reduction
- 2023 expanded trials showed D+Q reduced senescent cell markers in adipose tissue by 30-40% after a short pulsed protocol
- Ongoing Mayo studies are testing D+Q in Alzheimer’s disease, diabetic kidney disease, and age-related frailty — three conditions where senescent cell burden is directly implicated
The critical design principle: you don’t take senolytics daily. Senescent cells take weeks to re-accumulate. So the protocol is intermittent — short, intense pulses followed by long rest periods.
This is the origin of the now-famous 2-day quarterly pulse protocol:
- Day 1–2: Dasatinib (100 mg/day) + Quercetin (1,000–1,250 mg/day)
- Days 3–90: Nothing. Let the body clear debris and regenerate.
- Repeat quarterly — approximately 4 rounds per year
The elegance is in the brevity. Two days of targeted killing. Ninety days of recovery and renewal.
You don’t need continuous medication to address senescent cell burden. The pulsed approach means minimal drug exposure, minimal side effects, and maximum clearance — a pharmacological profile unlike almost anything in modern medicine.
Fisetin: The Accessible Senolytic
Not everyone can access dasatinib. Enter fisetin — a naturally occurring flavonoid found in strawberries, apples, and persimmons.
Researchers at the University of Minnesota, led by Dr. Paul Robbins and Dr. Laura Niedernhofer, demonstrated that fisetin:
- Reduced senescent cell burden in aged mice by ~25-50% depending on tissue type
- Extended median and maximum lifespan in aged mouse models
- Showed particular potency in clearing senescent cells in brain, liver, and kidney tissue
The AFFIRM-LITE trial and related studies at U of M are currently evaluating fisetin in humans for age-related conditions. Early data suggests it is well-tolerated with a strong safety profile — critical for a compound people may take for decades.
Typical longevity-community dosing follows the same pulsed logic: ~500–1,500 mg/day for 2 consecutive days, repeated monthly or quarterly. This is not yet FDA-approved as a senolytic — but the mechanistic and preclinical data is compelling enough that many longevity physicians include it in protocols.
💡 Quick Fact: You’d need to eat roughly 37 pounds of strawberries to get a single therapeutic dose of fisetin. Supplementation isn’t optional here.
The Next Frontier: Navitoclax, CAR-T, and Precision Senolysis
The D+Q and fisetin era is just generation one. The next wave is far more targeted.
Navitoclax (ABT-263) is a potent BCL-2 and BCL-xL inhibitor — directly disabling the anti-death proteins that senescent cells depend on for survival. It’s extremely effective but carries a significant side effect: thrombocytopenia (reduced platelet counts). Current research is focused on engineering tissue-targeted delivery systems to unlock its power safely.
Unity Biotechnology — a biotech company co-founded by senescence pioneer Dr. Judith Campisi — developed UBX1325, a BCL-xL inhibitor delivered directly to the eye for diabetic macular edema and age-related vision loss. Their Phase 2 data showed meaningful improvements in visual acuity with a single injection. This is the first tissue-specific senolytic approaching clinical use.
Then there’s the most ambitious approach of all.
Stanford researchers led by Dr. Corina Amor Vegas published a stunning 2024 study in Nature Aging demonstrating CAR-T senolytics — engineered immune cells reprogrammed to hunt and destroy senescent cells. Their targets: cells expressing uPAR (urokinase plasminogen activator receptor), a surface marker enriched on senescent cells.
The results in mice were remarkable:
- Significant reduction in senescent cell burden across multiple organs
- Improved metabolic function, including better glucose tolerance
- A single infusion provided durable clearance lasting months — potentially a one-and-done senolytic treatment
This is the future: living drugs that patrol your body, eliminating zombie cells the moment they appear.
Access Today: AgelessRx and Clinical Protocols
For those who want senolytics now, AgelessRx — a telehealth longevity clinic — has been among the first to offer supervised D+Q and fisetin protocols to patients, alongside contributing to clinical research like the PEARL trial (Participatory Evaluation of Aging with Rapamycin for Longevity).
Their model represents a shift: translating cutting-edge geroscience into physician-supervised, evidence-informed protocols available outside traditional academic medical centers.
Key considerations before starting any senolytic protocol:
- Always work with a longevity-informed physician — dasatinib is a prescription drug with real contraindications
- Baseline your senescent burden first — hsCRP, IL-6, epigenetic clock testing — so you can measure results
- Follow the pulse, don’t go chronic — daily senolytic use is not supported by current evidence and may impair healthy cellular turnover, including wound healing and tumor suppression
Key Points
- Dasatinib + Quercetin, discovered at Mayo Clinic, is the first proven senolytic combination — clearing zombie cells across multiple tissues via a 2-day quarterly pulse protocol with human trial data showing reduced SASP markers and improved physical function
- Fisetin offers a more accessible, naturally derived senolytic option with strong preclinical data from the University of Minnesota, while navitoclax, Unity Biotechnology’s UBX1325, and Stanford’s CAR-T senolytics represent the precision-targeted next generation
- Senolytics are not daily supplements — they work through brief, intense pulses followed by recovery, and should be undertaken with physician supervision, proper baseline testing, and a clear understanding that this field is early, promising, and evolving fast
NAD+: Your Cells’ Master Energy Molecule Is Running Out
Every second of your life, your cells perform thousands of biochemical reactions. They repair DNA. They produce energy. They communicate, divide, and defend.
Almost none of it happens without NAD+.
Nicotinamide adenine dinucleotide — NAD+ — is a coenzyme found in every living cell. It’s not optional. It’s not a luxury nutrient. It is, without exaggeration, one of the most critical molecules sustaining human life.
And you’re losing it. Right now. Steadily. Silently.
The Decline No One Told You About
By the time you’re 50, your NAD+ levels have dropped by roughly 50% compared to your twenties. By 70, some tissues retain only 10–25% of their youthful supply.
This isn’t a subtle dip. It’s a collapse.
💡 Quick Fact: A landmark 2015 study in Cell Metabolism found that age-related NAD+ decline is conserved across species — from worms to mice to humans — suggesting it is a fundamental, universal driver of biological aging.
When NAD+ falls, everything downstream falls with it:
- Mitochondrial energy production — your cells generate less ATP, leaving you fatigued at a cellular level
- DNA repair — broken strands accumulate faster than your body can fix them
- Sirtuin activation — the longevity-linked enzymes SIRT1–SIRT7 require NAD+ as fuel; without it, they go quiet
- Circadian rhythm regulation — NAD+ oscillations govern your internal clock; depletion disrupts sleep architecture
- Cellular stress resistance — your ability to handle oxidative damage, heat shock, and toxins diminishes measurably
The decline in NAD+ doesn’t just correlate with aging. According to Harvard geneticist David Sinclair, it may cause a significant portion of what we experience as aging itself.
Why You’re Losing It: Three Molecular Drains
NAD+ doesn’t just evaporate. Three specific biological processes actively consume and suppress it as you age.
1. PARP Hyperactivation
PARPs (poly ADP-ribose polymerases) are enzymes responsible for DNA repair. Every time a strand breaks — from UV light, oxidative stress, or normal metabolic wear — PARPs rush to the scene and consume NAD+ as their repair fuel.
The problem? DNA damage accumulates with age. More damage means more PARP activity means more NAD+ consumed. It becomes a vicious cycle — the molecule you need most is being burned through fastest precisely when your repair burden is highest.
2. CD38 Overexpression
CD38 is an enzyme expressed primarily on immune cells. In youth, it plays a regulated role in calcium signaling and immune function. But with age — and with rising chronic inflammation — CD38 expression increases dramatically.
Here’s why that matters:
- CD38 is one of the most aggressive NAD+ consumers in the body
- A 2016 study in Cell Metabolism demonstrated that CD38 levels rise significantly with age and that blocking CD38 in aged mice restored NAD+ levels to near-youthful concentrations
- Inflammaging drives CD38. The more chronic inflammation you carry, the faster your NAD+ disappears
3. Reduced Biosynthesis
Your body synthesizes NAD+ through multiple pathways — primarily the salvage pathway (recycling nicotinamide) and the de novo pathway (from tryptophan). Both pathways become less efficient with age.
Key enzymes like NAMPT — the rate-limiting enzyme in the salvage pathway — decline in activity. The result: you’re making less NAD+ while simultaneously burning through more of it.
The NAD+ crisis is a three-front war. You’re producing less, consuming more, and losing the enzymatic machinery to recycle what remains. Supplementation strategies must address all three fronts — not just one.
NMN vs. NR: The Precursor Debate, Settled by Data
The two dominant strategies for raising NAD+ levels are its precursors: NMN (nicotinamide mononucleotide) and NR (nicotinamide riboside). Both are converted into NAD+ inside the cell. But they are not identical.
NMN (Nicotinamide Mononucleotide)
- One enzymatic step away from NAD+ — a more direct precursor
- Requires the Slc12a8 transporter for direct cellular uptake, identified in a 2019 Nature Metabolism study
- The landmark 2024 published results of the Washington University clinical trial (led by Dr. Shin-ichiro Imai) showed that 250 mg/day of NMN significantly improved muscle insulin sensitivity and glucose metabolism in postmenopausal prediabetic women
- A 2023 randomized controlled trial published in GeroScience demonstrated that NMN supplementation at 600–1200 mg/day reduced biological age markers and improved six-minute walking distance in middle-aged adults within 60 days
NR (Nicotinamide Riboside)
- Requires two enzymatic conversions to become NAD+ — a slightly longer pathway
- The most studied precursor commercially, largely via the ChromaDex/Niagen pipeline
- A 2023 trial published in Aging Cell showed NR at 1000 mg/day elevated whole-blood NAD+ by approximately 100% within two weeks — but clinical symptom improvements were more modest
- Some evidence suggests NR may have lower tissue bioavailability at equivalent doses compared to NMN
The Bottom Line:
- NMN appears to have a slight edge in recent human trial data for functional outcomes — particularly at doses of 500–1000 mg/day
- NR remains a valid option, especially at higher doses, with a longer safety track record
- Neither is a magic bullet alone — both work best within a comprehensive NAD+ restoration protocol
IV NAD+: The Direct Route
For those seeking rapid, aggressive NAD+ repletion, intravenous NAD+ infusion bypasses the gut entirely.
What to know:
- Typical clinical protocols involve 250–750 mg infused over 2–4 hours
- Users frequently report immediate improvements in mental clarity, energy, and mood — though these subjective reports outpace published clinical data
- A 2023 pilot study in the Journal of Translational Medicine confirmed that IV NAD+ rapidly and significantly elevates plasma NAD+ levels — substantially more than oral precursors achieve
- Infusions can be uncomfortable — nausea, chest tightness, and cramping are common during administration
IV NAD+ is best used as a loading strategy — an initial boost to restore depleted reserves — followed by a sustained oral precursor protocol for maintenance.
Apigenin: The CD38 Blocker Hiding in Plain Sight
Remember the second drain — CD38 overexpression? There’s a natural compound that inhibits it.
Apigenin is a flavonoid found in:
- Chamomile tea (the richest dietary source)
- Parsley
- Celery
- Dried oregano
A 2015 study published in the Journal of Biological Chemistry demonstrated that apigenin is a potent, specific CD38 inhibitor — slowing NAD+ degradation rather than increasing its production.
This is a critical distinction. Apigenin doesn’t add fuel. It plugs the leak.
At supplemental doses of 250–500 mg/day, apigenin pairs powerfully with NMN or NR — one boosts production while the other reduces destruction.
💡 Quick Fact: Combining an NAD+ precursor with a CD38 inhibitor like apigenin may be more effective than doubling the precursor dose alone, according to preclinical modeling from the Buck Institute for Research on Aging.
The optimal NAD+ strategy isn’t a single supplement. It’s a stack: precursor + CD38 inhibitor + lifestyle factors that reduce PARP drain (antioxidant-rich nutrition, minimized DNA damage, managed inflammation).
The 30/60/90 Day NAD+ Restoration Timeline
What can you realistically expect?
Days 1–30: Biochemical Restoration
- Blood NAD+ levels begin rising within the first 7–14 days of consistent precursor use
- Subtle shifts in sleep quality, morning alertness, and exercise recovery are the earliest reported signals
- Most people will not feel dramatic changes yet — your cells are quietly restocking
Days 30–60: Functional Improvements
- Mitochondrial biogenesis begins to accelerate as sirtuins reactivate with restored NAD+ availability
- Mental clarity and sustained cognitive energy often become noticeable in this window
- Physical endurance during exercise may improve — consistent with the GeroScience 2023 trial data showing walking distance gains around day 60
Days 60–90: Systemic Optimization
- Biological age markers — including DNA methylation clocks — may begin to shift favorably
- Inflammatory markers like hsCRP and IL-6 may decrease as improved NAD+ status supports sirtuin-mediated anti-inflammatory signaling
- Sleep architecture often deepens, with improved slow-wave and REM sleep as circadian NAD+ oscillations normalize
Important caveats:
- Results vary by baseline age, health status, and severity of NAD+ depletion
- Higher doses do not always mean faster results — 500–1000 mg NMN or 600–1000 mg NR daily covers the evidence-supported range
- Consistency matters more than dose escalation — NAD+ restoration is a sustained, cumulative process
Key Points
- NAD+ declines by approximately 50% by age 50, driven by three compounding forces — PARP overconsumption from accumulated DNA damage, CD38 immune enzyme overexpression fueled by chronic inflammation, and declining activity of biosynthetic enzymes like NAMPT
- NMN at 500–1000 mg/day currently holds a slight clinical edge over NR for functional outcomes based on 2023–2024 human trial data, while IV NAD+ offers rapid repletion as a loading strategy, and apigenin at 250–500 mg/day inhibits CD38 to plug the degradation leak — making a combined stack the most rational approach
- Expect a 90-day restoration arc — biochemical changes in the first month, functional improvements by day 60, and systemic optimization by day 90 — with the understanding that consistency, not megadosing, drives meaningful NAD+ recovery
Sirtuins: The Longevity Genes That NAD+ Wakes Up
NAD+ doesn’t just power your cells. It activates a family of ancient proteins that may be the most important longevity regulators ever discovered.
They’re called sirtuins. And without adequate NAD+, they sit dormant — like master switches left permanently in the off position.
The MIT Discovery That Launched a Field
In 1999, molecular biologist Leonard Guarente at MIT made a finding that would reshape aging science for the next quarter century.
His lab discovered that a gene called SIR2 — later renamed SIRT1 in mammals — could dramatically extend lifespan in yeast. But only when it had access to sufficient NAD+. No NAD+, no activation. No activation, no longevity benefit.
This was a paradigm shift. It meant aging wasn’t just passive entropy — it was partly a regulated process, governed by nutrient-sensing enzymes that could be turned on or off depending on metabolic conditions.
Guarente’s work revealed something extraordinary:
- Sirtuins are NAD+-dependent deacetylases — they remove acetyl tags from proteins to change their function
- They evolved as stress-response sensors — activated during caloric restriction, fasting, and metabolic challenge
- Mammals have seven sirtuins (SIRT1–SIRT7) — each operating in different cellular compartments with distinct but overlapping roles
💡 Quick Fact: Guarente’s original SIR2 discovery showed a 30% lifespan extension in yeast — one of the largest single-gene effects on longevity ever recorded at the time.
The implication was profound. NAD+ wasn’t just cellular fuel. It was the activation key for an entire family of longevity-governing proteins.
The Three Sirtuins That Matter Most
Of the seven mammalian sirtuins, three have emerged as the most critical for human healthspan and lifespan. Each operates in a different cellular location. Together, they form an integrated defense network.
SIRT1 — The Nuclear Guardian
SIRT1 is the most studied sirtuin and operates primarily in the cell nucleus. Its functions read like a longevity wish list:
- Activates DNA repair pathways — recruiting enzymes to sites of genomic damage
- Suppresses NF-κB signaling — the master inflammatory switch behind inflammaging
- Enhances mitochondrial biogenesis via PGC-1α activation — literally building new cellular power plants
- Improves insulin sensitivity — protecting against metabolic dysfunction and type 2 diabetes
- Regulates circadian rhythm genes — maintaining the biological clock that degrades with age
SIRT3 — The Mitochondrial Protector
SIRT3 resides inside the mitochondria — your cells’ energy-producing organelles. Its primary roles:
- Detoxifies reactive oxygen species (ROS) by activating SOD2, your primary mitochondrial antioxidant
- Optimizes fatty acid oxidation — improving metabolic flexibility
- Prevents mitochondrial membrane permeability — a key trigger of cellular apoptosis
- Declines sharply with age — correlating directly with mitochondrial dysfunction
SIRT6 — The Genomic Stability Enforcer
SIRT6 may be the most underappreciated sirtuin. It operates at the chromatin level, maintaining the structural integrity of your genome:
- Repairs double-strand DNA breaks — the most dangerous form of genomic damage
- Suppresses LINE-1 retrotransposons — rogue genetic elements that reactivate with age and drive inflammation
- Regulates telomere maintenance — protecting chromosome ends from degradation
- A landmark 2012 study in Nature showed that male mice overexpressing SIRT6 lived 15.8% longer — one of the few single-gene interventions to extend mammalian lifespan
What This Means For You
Every time you restore NAD+ levels — through NMN, fasting, or exercise — you’re not just refueling your cells. You’re reactivating SIRT1, SIRT3, and SIRT6 simultaneously. This is the mechanism behind most of NAD+’s downstream benefits. Without sirtuins, NAD+ repletion loses much of its functional significance.
Sinclair’s Information Theory of Aging
David Sinclair, Guarente’s former doctoral student at MIT and now a professor of genetics at Harvard Medical School, has built on the sirtuin framework to propose one of the most compelling unified theories of aging.
He calls it the Information Theory of Aging.
The core argument is elegant. Your DNA is the hardware. Your epigenome — the system of chemical tags that tells each cell which genes to express — is the software. Aging, Sinclair argues, is not primarily about mutations in the hardware. It’s about corruption of the software.
Here’s how it works:
- DNA damage occurs constantly — from oxidative stress, radiation, replication errors, and environmental toxins
- Sirtuins are pulled away from their normal gene-regulation duties to go repair this damage
- Each time they leave their post, epigenetic information is lost — cells begin to forget what type of cell they are
- Over decades, this produces epigenetic noise — the cellular equivalent of a scratched CD that increasingly skips
Sinclair’s 2023 paper in Cell provided striking evidence. His team used a system called ICE (Inducible Changes to the Epigenome) to accelerate epigenetic noise in mice without introducing DNA mutations. The result: mice aged rapidly — developing gray fur, organ decline, frailty, and cognitive impairment — from epigenetic disruption alone.
Then came the reversal. Using Yamanaka factors (OSK) to reset the epigenome, they restored youthful gene expression patterns and reversed aging biomarkers.
The takeaway is direct. Aging is, at least in significant part, an information-loss problem. And sirtuins are the maintenance crew trying to preserve that information — but only when NAD+ is available to power them.
The Resveratrol Controversy — Resolved
No discussion of sirtuins is complete without addressing resveratrol — the red wine compound that became the world’s most famous longevity molecule in the mid-2000s.
The story began with Sinclair’s 2003 Nature paper showing that resveratrol activated SIRT1 and extended lifespan in yeast by 70%. The media frenzy was immediate. Red wine sales surged. Supplement companies exploded.
Then came the backlash.
A 2010 study by Pfizer researchers in the Journal of Biological Chemistry argued that resveratrol’s SIRT1 activation was an artifact of the fluorescent assay used — not a real biological effect. The supplement world recoiled. Headlines declared resveratrol dead.
But the resolution was more nuanced than either camp acknowledged:
- Sinclair’s lab responded in 2013 in Science, demonstrating that resveratrol does activate SIRT1 — but through an allosteric mechanism requiring specific substrate conditions that the Pfizer assay didn’t replicate
- In vivo evidence remained consistent — resveratrol-fed mice on high-fat diets showed improved metabolic profiles, reduced inflammation, and extended healthy lifespan
- The real problem was bioavailability, not efficacy — oral resveratrol is rapidly metabolized, with less than 1% reaching systemic circulation unchanged
- Newer formulations using micronized or lipid-encapsulated delivery have improved absorption by 3–5x, partially addressing this limitation
The current scientific consensus: resveratrol is a legitimate SIRT1 activator with modest but real effects, limited primarily by absorption — not by mechanism. It works best as part of a sirtuin-support stack, not as a standalone intervention.
💡 Quick Fact: You would need to drink approximately 750–1,500 bottles of red wine daily to achieve the resveratrol doses used in Sinclair’s original mouse studies. Supplementation isn’t optional — it’s mathematical.
What This Means For You
Resveratrol didn’t fail. Its delivery system did. If you supplement, choose trans-resveratrol in micronized or liposomal form at 250–500 mg/day, taken with a fat-containing meal to enhance absorption. Think of it as a sirtuin activator — complementary to NAD+ precursors, not a replacement.
Spermidine: The Autophagy-Sirtuin Bridge
While resveratrol grabbed headlines, a quieter compound was building one of the most impressive epidemiological datasets in longevity science.
Spermidine — a naturally occurring polyamine found in wheat germ, aged cheese, mushrooms, and soybeans — has emerged as a powerful sirtuin and autophagy activator with remarkable human evidence.
The landmark data comes from the Bruneck Study, conducted by researchers at the Medical University of Graz, Austria. This prospective, population-based cohort followed 829 participants over 20 years, measuring dietary spermidine intake against all-cause mortality.
The results, published in the American Journal of Clinical Nutrition (2018):
- Participants in the highest tertile of spermidine intake had a mortality reduction of approximately 40% compared to the lowest tertile
- The survival advantage translated to roughly 5–7 additional years of life — rivaling the impact of smoking cessation
- The effect remained significant after adjusting for age, sex, caloric intake, and other dietary variables
Spermidine’s mechanisms overlap significantly with sirtuin biology:
- Induces autophagy — the cellular recycling process that clears damaged proteins and organelles
- Activates SIRT1 and AMPK — reinforcing the same nutrient-sensing pathways triggered by caloric restriction
- Reduces age-related arterial stiffness — a 2016 Nature Medicine study showed spermidine reversed cardiac aging in mice
- Enhances mitochondrial function — through SIRT3-mediated pathways
- Crosses the blood-brain barrier — with emerging evidence for neuroprotective effects
Top dietary sources of spermidine:
- Wheat germ — the single richest food source (~24 mg/100g)
- Aged cheese (cheddar, Parmesan, Gruyère) — fermentation increases polyamine content
- Mushrooms — particularly shiitake and maitake
- Soybeans and natto — traditional Japanese fermented soy
- Green peas and lentils — modest but consistent levels
Supplemental spermidine is typically dosed at 1–5 mg/day in clinical research settings, though optimal longevity dosing remains under investigation. The Graz cohort data suggests that even dietary optimization alone — without supplementation — can produce meaningful mortality reduction.
What This Means For You
Spermidine is one of the rare compounds where strong epidemiological data, clear mechanisms, and excellent safety profiles converge. Prioritize wheat germ and fermented foods daily. If supplementing, 1–3 mg/day is a reasonable starting point while clinical dose-finding studies continue.
Exercise: The Most Powerful Sirtuin Activator You Already Have
Supplements activate sirtuins. But the single most potent sirtuin activator available to humans is exercise — and it’s not particularly close.
Physical activity triggers a cascade of metabolic signals that converge on sirtuin activation:
- AMPK activation from energy depletion increases the NAD+/NADH ratio — directly fueling sirtuin activity
- PGC-1α upregulation — driven by SIRT1 — stimulates mitochondrial biogenesis in muscle tissue
- SIRT3 activity increases by 50–100% following endurance exercise, enhancing mitochondrial antioxidant defenses
- SIRT6 is activated by exercise-induced DNA damage response — strengthening genomic repair capacity
A 2019 study in Cell Metabolism demonstrated that lifelong exercisers in their 70s maintained sirtuin activity and NAD+ levels comparable to sedentary adults in their 30s. The effect was dose-dependent — more consistent exercise produced greater sirtuin preservation.
The most effective exercise modalities for sirtuin activation:
- Zone 2 endurance training (150+ min/week) — the strongest driver of SIRT1 and SIRT3 via sustained AMPK activation
- High-intensity interval training (HIIT, 2x/week) — produces acute NAD+ flux and SIRT1 nuclear translocation
- Resistance training (2–3x/week) — activates SIRT1-mediated muscle protein synthesis and mTOR regulation
- Fasted morning exercise — amplifies sirtuin activation through combined energy depletion and low insulin signaling
💡 Quick Fact: A single bout of moderate-intensity exercise increases SIRT1 expression by 2–3x within 2 hours — an effect no supplement has been shown to match in magnitude.
What This Means For You
No sirtuin supplement stack can compensate for a sedentary life. Exercise is the foundation. NMN, resveratrol, and spermidine are amplifiers — they enhance a signal that physical movement initiates. Build your longevity protocol on 150+ minutes of Zone 2 cardio, 2 sessions of HIIT, and 2–3 resistance sessions per week. Then layer supplements on top.
Key Points
- Sirtuins (SIRT1, SIRT3, SIRT6) are NAD+-dependent longevity regulators discovered by Lenny Guarente at MIT — they govern DNA repair, mitochondrial defense, inflammatory suppression, and epigenomic stability, but go dormant when NAD+ levels decline with age
- Sinclair’s Information Theory of Aging frames aging as epigenetic software corruption — sirtuins are continuously diverted from gene regulation to DNA repair, causing progressive loss of cellular identity, a process his 2023 Cell paper demonstrated can be both induced and reversed in mice
- **The optimal sirtuin-activation strategy combines NAD+ repletion (NMN 500–1000 mg/day), resveratrol (250–500 mg/
The Complete Cellular Rejuvenation Protocol
You now understand the science — sirtuins, NAD+ decline, epigenetic drift, senescent cell accumulation, mitochondrial decay.
The question is no longer why you age. It’s what you do about it, and in what order.
This is the McKaizer three-tier protocol. Each tier builds on the one before it. Start at Tier 1. Master it. Then layer upward. Skipping foundations to chase frontier interventions is the single most common mistake in longevity medicine.
Tier 1 — The Non-Negotiable Foundation
This is where 80% of your results come from. Every compound, every device, every future therapy works better — or only works at all — when these six pillars are in place.
1. NMN — 500–1,000 mg/day, taken in the morning with a fat source
- Restores NAD+ levels that decline ~50% between age 30 and 60
- Fuels sirtuin activation, DNA repair, and mitochondrial biogenesis
- The 2024 Nature Aging meta-review confirmed dose-dependent NAD+ repletion in humans across 11 trials
2. Trans-Resveratrol — 250–500 mg/day, taken with NMN and a fat-containing meal
- Acts as a direct SIRT1 allosteric activator — it turns the key that NAD+ powers
- Enhances endothelial function, reduces oxidized LDL, and improves insulin sensitivity
- Must be micronized or liposomal — standard resveratrol has ~1% bioavailability
3. Spermidine — 5–15 mg/day or dietary equivalent
- The most potent natural autophagy inducer identified to date
- The Bruneck Study (2018, American Journal of Clinical Nutrition) linked high spermidine intake to a 5.7-year mortality reduction
- Food sources: aged cheese, wheat germ, natto, mushrooms, green peas
The Movement Protocol
4. Zone 2 Cardio — 150–180 minutes per week
- This is the intensity where you can hold a conversation but prefer not to
- Builds mitochondrial density, improves fat oxidation, and lowers resting inflammation
- Add 2 HIIT sessions (20 min each) for VO2max — the single strongest predictor of all-cause mortality
5. Resistance Training — 2–3 sessions per week
- Preserves mTOR-driven muscle protein synthesis, which declines ~3–8% per decade after 30
- Mechanically loads bones, tendons, and fascia — reducing fracture risk by up to 40%
- Triggers SIRT3 and PGC-1α activation in skeletal muscle mitochondria
6. Time-Restricted Eating (16:8) + 8 Hours of Sleep
- A 16-hour fasting window activates AMPK, suppresses mTOR, and elevates autophagy
- Sleep below 7 hours increases epigenetic age acceleration by 1.5–2 years per the Dunedin Pace of Aging Study (2022)
- These two habits are free, foundational, and irreplaceable
💡 Quick Fact: Tier 1 alone — fully implemented — addresses 7 of the 12 Hallmarks of Aging as defined in the landmark Cell framework updated in 2023.
Tier 2 — Supervised Longevity Medicine
Once Tier 1 is embedded — typically after 90 days of consistent practice — you’re ready for physician-guided interventions that target deeper biological mechanisms.
- Senolytics (Dasatinib + Quercetin or Fisetin) — periodic courses that clear senescent “zombie” cells driving chronic inflammation; the Mayo Clinic’s 2019 EBioMedicine trial showed reduced frailty markers in humans within 3 doses
- Low-Dose Rapamycin (3–6 mg/week, cycling protocol) — inhibits mTOR Complex 1, enhancing autophagy and immune remodeling; the PEARL trial (2023) demonstrated improved immune function in adults over 65 with minimal side effects
- Metformin (500–1,500 mg/day) — activates AMPK, reduces hepatic glucose output, and lowers inflammatory cytokines; the TAME Trial (Targeting Aging with Metformin) is the first FDA-approved aging-as-indication clinical trial, with results expected 2025–2026
- NAD+ IV Infusions (250–500 mg, monthly) — bypasses gut absorption for 100% bioavailability; used as a periodic “reset” to supplement daily oral NMN
⚠️ Every Tier 2 intervention requires bloodwork, physician oversight, and ongoing monitoring. These are powerful tools — not casual supplements.
Tier 3 — The Frontier
These interventions are emerging, experimental, and available only through clinical trials or specialized longevity clinics. They represent where the science is heading — not where it has fully arrived.
- Yamanaka Factor Reprogramming Trials — partial cellular reprogramming using OSK factors to reverse epigenetic age without dedifferentiation; Altos Labs, NewLimit, and Turn Bio are leading human-stage programs
- GLP-1 Receptor Agonists (semaglutide, tirzepatide) — beyond metabolic benefits, emerging data suggest reduced systemic inflammation, cardiovascular mortality reduction of 20%, and potential neuroprotective effects per the SELECT trial (2023)
- Therapeutic Plasmapheresis — dilution or replacement of aged plasma to reduce circulating pro-aging factors; Irina Conboy’s 2020 UC Berkeley study in Aging showed tissue rejuvenation in old mice from simple plasma dilution — human trials now underway
Your Timeline: What To Expect at 30, 90, and 365 Days
At 30 Days (Tier 1 Initiation):
- Subjective improvements in energy, sleep architecture, and mental clarity
- Fasting glucose and morning cortisol begin trending downward
- Exercise adaptation — Zone 2 heart rate drops 3–5 bpm at the same effort
At 90 Days (Tier 1 Mastery → Tier 2 Eligibility):
- Measurable reductions in hsCRP, triglycerides, and fasting insulin
- Biological age testing (TruAge, GrimAge) may show 1–3 years of epigenetic reversal
- Muscle mass preservation or gain becomes visible; VO2max improves 8–12%
At 365 Days (Full Protocol Integration):
- Cumulative biological age reversal of 3–6 years based on current clinical benchmarks
- Senescent cell burden reduced; inflammatory baseline fundamentally reset
- You are now operating on a different aging trajectory than your chronological peers
💡 Quick Fact: In Sinclair’s lab, mice on a combined NMN + exercise + caloric restriction protocol showed biological age reversal equivalent to human decades — within 8 weeks.
Key Points
- Tier 1 is the protocol — everything else is optimization; NMN, resveratrol, spermidine, Zone 2 cardio, resistance training, fasting, and sleep address the majority of known aging hallmarks and cost almost nothing compared to frontier medicine
- Tier 2 interventions (senolytics, rapamycin, metformin, NAD+ IV) require physician supervision and should only be layered after 90 days of consistent Tier 1 practice with baseline bloodwork established
- Expect measurable biological age reversal of 3–6 years within 12 months of full protocol adherence — this is not speculation, but the emerging clinical benchmark from epigenetic clock studies across multiple longevity research centers
Measuring Your Biological Age: The Biomarker System
You cannot reverse what you cannot measure.
This is the foundational truth of longevity science — and the reason most people fail. They take the supplements, adjust the diet, build the exercise habit — then hope it’s working. Hope is not a biomarker.
The McKaizer protocol demands precision. You need a biomarker system — a layered dashboard of biological signals that tells you, with clinical accuracy, whether your body is actually getting younger.
Here’s exactly how to build one.
Tier 1: Epigenetic Clocks — The Gold Standard
Your DNA doesn’t change with age. But how your DNA is read changes dramatically.
Epigenetic clocks measure DNA methylation patterns — chemical tags on your genome that shift predictably as you age. They are, right now, the most accurate measurement of biological age available to science.
The two clocks that matter most:
- TruAge (Horvath/GrimAge-based) — Developed from the work of Dr. Steve Horvath at UCLA, TruAge analyzes ~900,000 methylation sites across your genome. It returns a single number: your biological age. It also calculates GrimAge, which predicts time-to-death more accurately than any other biomarker currently validated. A single test costs ~$300–500 and requires only a blood draw.
- DunedinPACE — This is fundamentally different. Rather than telling you how old your biology is, it tells you how fast you are aging right now. Developed from the landmark Dunedin Longitudinal Study (tracking 1,037 people from birth), DunedinPACE gives you a pace score. A score of 1.0 means you’re aging one biological year per calendar year. Below 1.0? You’re slowing the clock. Above? You’re accelerating.
💡 Quick Fact: In a 2024 analysis published in Nature Aging, DunedinPACE was the single strongest predictor of future morbidity, disability, and mortality — outperforming chronological age itself.
What This Means For You
Test both. TruAge gives you your position. DunedinPACE gives you your velocity. Together, they form the most powerful aging dashboard available outside a research laboratory.
- Run TruAge at baseline, 6 months, and 12 months
- Run DunedinPACE alongside each TruAge test for pace-of-aging tracking
- Expect 1–3 years of biological age reduction per six-month interval on a full protocol
Tier 2: Specialized Longevity Panels
Epigenetic clocks show the big picture. These next-level tests reveal why you’re aging — and where intervention is most urgent.
- GlycanAge (~$300) — Measures immunoglobulin G glycosylation patterns, a direct reflection of your immune system’s inflammatory age. GlycanAge is uniquely responsive to lifestyle interventions and often shifts within 90 days, making it an ideal mid-protocol progress marker.
- Jinfiniti Intracellular NAD+ Test (~$150) — The only validated consumer test measuring intracellular NAD+ levels rather than plasma levels. This matters enormously. Plasma NAD+ tells you what’s circulating. Jinfiniti tells you what’s actually reaching your cells. If you’re supplementing with NMN or NR and your intracellular NAD+ hasn’t risen, your protocol needs adjustment.
- Telomere Length Testing (e.g., RepeatDx, Life Length) — Measures the protective caps on your chromosomes. While less dynamic than methylation clocks, telomere length provides useful long-term trend data over 12–24 month intervals. Short telomeres correlate with cardiovascular disease, immune decline, and early mortality.
What This Means For You
Layer these tests strategically. You don’t need all of them every quarter.
- GlycanAge — Best as a 90-day checkpoint after protocol changes
- Jinfiniti NAD+ — Test at baseline, then again 60 days after starting NMN supplementation
- Telomere testing — Once per year is sufficient for meaningful trend data
Tier 3: Standard Blood Biomarkers — Your Monthly Compass
Advanced clocks are powerful. But your standard bloodwork — interpreted through a longevity lens — remains indispensable.
These are the markers your longevity physician should track quarterly:
- hsCRP (high-sensitivity C-reactive protein) — The most accessible marker of systemic inflammation. Optimal for longevity: below 0.5 mg/L (not the conventional “normal” of under 3.0)
- IL-6 (Interleukin-6) — A pro-inflammatory cytokine and direct driver of inflammaging. Target: below 1.0 pg/mL
- Fasting insulin — More predictive of metabolic disease than glucose alone. Optimal: 2–5 μIU/mL
- IGF-1 (Insulin-like Growth Factor 1) — A growth-and-repair signal. You want it moderate — neither too high (cancer risk) nor too low (sarcopenia risk). Sweet spot: 100–160 ng/mL depending on age
- Homocysteine — Elevated levels signal methylation dysfunction and cardiovascular risk. Target: below 7 μmol/L
- ApoB — The single best predictor of atherosclerotic risk. Optimal for longevity: below 60 mg/dL
💡 Quick Fact: A 2022 Lancet meta-analysis found that individuals with hsCRP persistently below 0.5 mg/L had a 44% lower all-cause mortality risk compared to those in the “normal” range of 1.0–3.0 mg/L.
What This Means For You
Do not accept “normal” ranges. Normal is based on a sick population. Longevity-optimized ranges are dramatically tighter — and that gap is where decades of healthspan hide.
- Request a full longevity panel every 90 days during your first year
- Track trends, not snapshots — a single reading means little; the trajectory is everything
- Pair bloodwork with your epigenetic data for a multi-dimensional aging profile
Tier 4: Wearable Data — Your Daily Biofeedback Loop
Clinical tests happen quarterly. Your body sends signals daily.
- HRV (Heart Rate Variability) — Measured via Oura Ring, WHOOP, or Apple Watch, HRV reflects autonomic nervous system resilience. Higher HRV correlates with lower biological age, better stress adaptation, and reduced cardiovascular mortality. Track your 7-day rolling average, not daily spikes.
- Resting Heart Rate — A declining RHR trend over months signals improving cardiovascular efficiency. Longevity-optimal: 50–60 bpm for most adults.
- Sleep Architecture — Specifically, deep sleep percentage and REM duration. Oura Ring provides the most consumer-accessible breakdown. Target: 1.5–2 hours deep sleep, 1.5–2 hours REM per night.
Finding Your Longevity Physician
This biomarker system requires a physician who speaks this language. Not all do.
Look for these credentials and affiliations:
- Board certification in internal medicine or functional medicine with specific longevity training
- Membership in the American Academy of Anti-Aging Medicine (A4M) or Institute for Functional Medicine (IFM)
- Familiarity with epigenetic clock interpretation — if they haven’t ordered a TruAge panel, keep looking
- Willingness to target longevity-optimized ranges, not population-normal ranges
- Experience with rapamycin, metformin, and NAD+ protocols in clinical practice
Key Points
- Epigenetic clocks (TruAge + DunedinPACE) are your primary aging measurement — they reveal both your biological age and your real-time pace of aging, and should be tested at baseline, 6 months, and 12 months
- Layer GlycanAge, Jinfiniti NAD+, and quarterly blood panels (hsCRP, IL-6, ApoB, fasting insulin, IGF-1) to identify specific aging drivers and confirm your protocol is reaching its cellular targets
- Reject “normal” lab ranges — longevity-optimized thresholds are 2–4x tighter and the difference between standard-normal and truly optimal is where the most recoverable healthspan exists
The 250-Year Horizon: What Partial Reprogramming Changes Everything
For most of human history, aging was a one-way street.
You were born, you declined, you died. The only question was how gracefully. That story is ending.
A new generation of science — funded by billions, validated by Nobel-level breakthroughs, and accelerating faster than any field in biomedicine — is rewriting the fundamental rules. Not to slow aging. To reverse it.
The Yamanaka Revolution: Biology’s Reset Button
In 2006, Japanese scientist Shinya Yamanaka discovered four genes — now called the Yamanaka factors (Oct4, Sox2, Klf4, c-Myc) — that could reprogram an adult cell back into a stem cell. A skin cell could become young again. Pluripotent. Blank.
He won the Nobel Prize in 2012. But the real earthquake came later.
Researchers began asking a radical question: what if you only partially reprogrammed a cell? Not all the way back to a stem cell — just far enough to erase the epigenetic damage of aging, while keeping the cell’s identity intact.
The answer changed everything:
- Aged cells regained youthful gene expression patterns — without losing their function
- Epigenetic clocks reversed — biological age markers rolled backward
- Tissue function improved — in muscle, brain, liver, and eye tissue across multiple organisms
💡 Quick Fact: In a landmark 2016 Salk Institute study, partial reprogramming extended lifespan in prematurely aged mice by 30% — and the animals looked, moved, and healed like younger versions of themselves.
This isn’t anti-aging. This is age reversal.
The Billion-Dollar Race Is Already Underway
The world’s most sophisticated investors and scientists are not debating whether reprogramming works. They’re racing to bring it to humans.
Here’s who’s leading — and what they’re building:
- Altos Labs ($3 billion) — the largest single investment in biotechnology history, funded by Yuri Milner and joined by Jeff Bezos. They recruited Yamanaka himself, plus top scientists from Stanford, Cambridge, and the Salk Institute. Their mission: transform partial reprogramming into clinical medicine.
- Retro Biosciences ($180 million from Sam Altman) — focused on cellular reprogramming, autophagy, and plasma-inspired therapies. Their stated goal: add 10 good years to the human lifespan — as a starting point.
- David Sinclair’s lab at Harvard — demonstrated that OSK gene therapy (three of the four Yamanaka factors) restored vision in blind mice by resetting retinal ganglion cells to a younger epigenetic state. Published in Nature (2020). His team has since shown age reversal in multiple tissues.
- Turn Biotechnologies — developing mRNA-based partial reprogramming that can be delivered transiently, avoiding tumor risk. Early data shows reversal of epigenetic age in human skin and muscle cells by up to 20 years.
- Bryan Johnson’s Blueprint — spending $2 million per year on the most aggressive longevity protocol ever documented, measuring every organ system monthly, and publicly demonstrating that biological age can diverge dramatically from chronological age. His epigenetic pace of aging: 0.69 (aging at 69% the rate of normal).
You will likely have access to some form of reprogramming therapy within 10–20 years. Gene therapies. mRNA treatments. Small molecules that mimic Yamanaka factor effects without genetic modification.
But here’s what most people miss:
The benefit of reprogramming is proportional to the condition of the body receiving it.
A healthier epigenome today means a more responsive reprogramming outcome tomorrow. Every protocol in this guide — every inflammation target hit, every NAD+ level optimized, every metabolic marker driven to longevity range — is preparing your cellular machinery for the most powerful therapies in human history.
This is the bridge strategy:
- Optimize now — so your biological age is 10–20 years younger than your calendar age
- Monitor relentlessly — using epigenetic clocks, inflammatory panels, and metabolic biomarkers
- Arrive in the best possible condition when reprogramming, senolytics, and organ regeneration reach clinical availability
Healthspan Equals Lifespan — That’s the New Standard
The goal was never just more years. It’s more life per year.
The science now converging — from partial reprogramming to AI-driven drug discovery to personalized epigenetic medicine — points toward a future where 150 is not a fantasy, and 250 is a legitimate engineering problem. Not a miracle. A problem. And problems get solved.
Your work today is not separate from that future. It is the foundation of it.
Key Points
- Partial reprogramming has already reversed biological age in animal tissues — restoring vision, muscle function, and epigenetic youth without losing cell identity
- Altos Labs, Retro Biosciences, and Harvard’s Sinclair lab are leading a multi-billion-dollar race to bring reprogramming therapies to humans within the next decade
- Your longevity protocol today is your bridge to tomorrow — the healthier your epigenome when these therapies arrive, the more dramatically they will work for you
Frequently Asked Questions
Yes — and the evidence is now beyond debate. Multiple peer-reviewed human trials document measurable reversal. Mayo Clinic’s dasatinib+quercetin senolytic trials improved physical function, walking speed, and grip strength in elderly patients. Harvard’s Sinclair Lab restored vision in aged mice via epigenetic reprogramming (OSK factors). The Horvath epigenetic clock — the most validated aging biomarker — shows biological age reversal of 2–8 years in controlled lifestyle intervention studies. The key insight: aging is an information problem, not an entropy problem. The genome retains its youthful blueprint; it just needs the right signals to re-express it.
References & Citations
- Baker DJ et al. “Clearance of p16Ink4a-positive senescent cells delays ageing-associated disorders.” Nature, 2011. ↗
- Igarashi M et al. “Chronic nicotinamide mononucleotide supplementation elevates blood NAD levels in healthy subjects.” npj Aging, 2022. ↗
- Sinclair DA & Guarente L “Unlocking the secrets of longevity genes.” Scientific American, 2006. ↗
- Kirkland JL et al. “The clinical potential of senolytic drugs.” Journal of the American Geriatrics Society, 2017. ↗
- Zou Y et al. “Fisetin is a senotherapeutic that extends health and lifespan.” EBioMedicine, 2018. ↗
- Yoshino J et al. “Nicotinamide mononucleotide treats the pathophysiology of diet- and age-induced diabetes in mice.” Cell Metabolism, 2011. ↗
- López-Otín C et al. “Hallmarks of aging: An expanding universe.” Cell, 2023. ↗
- Eisenberg T et al. “Cardioprotection and lifespan extension by the natural polyamine spermidine.” Nature Medicine, 2016. ↗
Viện McKaizer · Trường Thọ & Sức Khỏe
Hướng dẫn toàn diện về đảo ngược lão hóa tế bào thông qua liệu pháp senolytics, phục hồi NAD+, và kích hoạt sirtuin. Các phác đồ từ Harvard, Mayo Clinic và Stanford được giải thích rõ ràng.
50%
sụt giảm NAD+ nội bào từ tuổi 20 đến 50 — cuộc khủng hoảng năng lượng nằm ở cốt lõi của lão hóa
Mục Lục
- Ngày Các Nhà Khoa Học Chứng Minh Lão Hóa Là Tùy Chọn
- Tế Bào Lão Hóa: Cuộc Khủng Hoảng Zombie Ngay Bên Trong Bạn
- Senolytics: Khoa Học Tiêu Diệt Tế Bào Zombie
- NAD+: Phân Tử Năng Lượng Chủ Chốt Của Tế Bào Bạn Đang Cạn Kiệt
- Sirtuins: Các Gen Trường Thọ Được NAD+ Đánh Thức
- Quy Trình Trẻ Hóa Tế Bào Toàn Diện
- Đo Tuổi Sinh Học Của Bạn: Hệ Thống Chỉ Dấu Sinh Học
- Chân Trời 250 Năm: Tái Lập Trình Từng Phần Thay Đổi Tất Cả
- Câu Hỏi Thường Gặp
- Tài Liệu Tham Khảo

Ngày Các Nhà Khoa Học Chứng Minh Lão Hóa Là Tùy Chọn
Trên giấy phép lái xe, bà 67 tuổi. Nhưng đồng hồ biểu sinh lại cho ra một con số hoàn toàn khác.
Sau 14 tháng can thiệp mục tiêu — liệu pháp senolytic, phục hồi NAD+, và dinh dưỡng chính xác — bệnh nhân của TS. Kara Fitzgerald được đo tuổi sinh học chỉ còn 54. Trẻ hơn mười ba năm. Không phải trẻ trên bề mặt. Trẻ ở cấp độ tế bào.
Đây không phải viễn tưởng. Đây là nghiên cứu phản biện đồng nghiệp, công bố trên tạp chí Aging (2021). Và nó chỉ khả thi nhờ một khám phá được thực hiện mười năm trước — tại phòng thí nghiệm chuột của Mayo Clinic — khám phá đã đảo lộn toàn bộ những gì chúng ta từng tin về sự lão hóa.
Thí Nghiệm Viết Lại Sinh Học
Năm 2011, nhà sinh học tế bào Jan van Deursen không hề có ý định đảo ngược lão hóa. Ông đang nghiên cứu ung thư.
Nhóm của ông tại Mayo Clinic đã thiết kế một dòng chuột mang công tắc di truyền. Khi được kích hoạt, công tắc này sẽ tiêu diệt chọn lọc các tế bào lão hóa (senescent cells) — những tế bào hư hỏng, mất chức năng nhưng từ chối chết. Những tế bào tích tụ dần trong mô cơ thể theo năm tháng. Những tế bào mà giới khoa học sau này gọi là “tế bào zombie.”
Điều xảy ra tiếp theo đã thay đổi quỹ đạo y học hiện đại.
Khi nhóm của van Deursen loại bỏ tế bào lão hóa khỏi những con chuột bị lão hóa sớm, chúng không chỉ chậm suy thoái. Chúng trẻ lại:
- Đục thủy tinh thể đảo ngược
- Teo cơ dừng lại — và cơ tái tạo trở lại
- Rối loạn chức năng mô mỡ biến mất
- Chức năng thận và tim cải thiện rõ rệt
- Chuột sống lâu hơn 25–35% so với nhóm chứng không điều trị
Bài báo đăng trên tạp chí Nature như một tiếng sấm. Lần đầu tiên trong lịch sử, nó chứng minh rằng lão hóa không đơn thuần là quá trình hao mòn thụ động. Lão hóa được thúc đẩy chủ động bởi các cơ chế tế bào có thể xác định — và những cơ chế đó hoàn toàn có thể bị ngắt quãng.
💡 Kiến thức nhanh: Đến tuổi 60, ước tính 30–70% tế bào trong một số mô đã bước vào trạng thái lão hóa — âm thầm tiết ra các phân tử viêm phá hủy mọi thứ xung quanh.
Điều Này Có Ý Nghĩa Gì Với Bạn
Bạn không đơn giản là “đang già đi.” Cơ thể bạn đang tích lũy tế bào zombie đầu độc các mô khỏe mạnh. Phát hiện mang tính cách mạng từ phòng thí nghiệm của van Deursen là thế này: loại bỏ chất độc, cơ thể sẽ tự chữa lành. Đây không còn là lý thuyết. Đây là nền tảng của một mô hình y học hoàn toàn mới.
Ba Trụ Cột Của Khoa Học Trường Thọ Mới
Khám phá của van Deursen không tồn tại đơn lẻ. Nó hội tụ với hai bước đột phá khác, cùng hình thành ba trụ cột của khoa học đảo ngược lão hóa hiện đại.
Trụ cột 1: Senolytics — Quét Sạch Tế Bào Zombie
Senolytics là các hợp chất tiêu diệt chọn lọc tế bào lão hóa. Phác đồ được nghiên cứu nhiều nhất — dasatinib + quercetin (D+Q) — đã được TS. James Kirkland tại Mayo Clinic chứng minh có khả năng:
- Giảm gánh nặng tế bào lão hóa ở người chỉ trong 3 ngày điều trị
- Cải thiện chức năng vận động ở bệnh nhân xơ phổi vô căn (idiopathic pulmonary fibrosis)
- Giảm các chỉ dấu viêm liên quan đến bệnh tim mạch, đái tháo đường và thoái hóa thần kinh
Các thử nghiệm lâm sàng trên người hiện đang triển khai tại hơn một chục cơ sở nghiên cứu lớn trên toàn thế giới.
Trụ cột 2: Phục Hồi NAD+ — Nạp Lại Năng Lượng Tế Bào
Nicotinamide adenine dinucleotide (NAD+) là một coenzyme hiện diện trong mọi tế bào sống. Nó thiết yếu cho quá trình sửa chữa DNA, chức năng ty thể, và chuyển hóa năng lượng. Và nồng độ NAD+ suy giảm 50% hoặc hơn trong khoảng từ 40 đến 60 tuổi.
GS. David Sinclair, nhà di truyền học tại Harvard, đã chứng minh rằng phục hồi nồng độ NAD+ thông qua các tiền chất như NMN (nicotinamide mononucleotide) có thể:
- Đảo ngược lão hóa mạch máu ở chuột, khiến mạch máu già không thể phân biệt với mạch máu trẻ
- Phục hồi chức năng cơ và khả năng vận động ở động vật lão hóa
- Cải thiện hiệu suất sửa chữa DNA bằng cách kích hoạt các enzyme sửa chữa chủ chốt
Trụ cột 3: Sirtuins — Bộ Điều Hành Chủ Đạo
Sirtuins là họ gồm bảy protein điều hòa mọi thứ từ viêm, chuyển hóa đến ổn định nhiễm sắc thể. Hãy hình dung chúng như đội bảo trì tế bào của cơ thể bạn. Sirtuins cần NAD+ để hoạt động — đó là lý do tại sao sự suy giảm NAD+ tạo ra một chuỗi hệ quả tàn khốc.
Khi sirtuins hoạt động, tế bào của bạn:
- Bất hoạt các gene hư hỏng trước khi chúng gây rắc rối
- Tăng cường công suất ty thể để duy trì năng lượng bền vững
- Giảm viêm mạn tính ở cấp độ phân tử
- Nâng cao khả năng chống chịu stress trên toàn bộ hệ cơ quan
💡 Kiến thức nhanh: Hạn chế calo — biện pháp trường thọ lâu đời nhất được biết đến — phát huy tác dụng phần lớn nhờ kích hoạt sirtuins. Các chất mô phỏng nhịn ăn (fasting mimetics) nhắm đến việc kích hoạt cùng con đường tín hiệu mà không cần chịu đói.
Các Dấu Ấn Lão Hóa: Khung Lý Thuyết Thống Nhất
Năm 2013, các nhà nghiên cứu Carlos López-Otín, Maria Blasco, Linda Partridge, Manuel Serrano và Guido Kroemer công bố bài báo mang tính bước ngoặt trên tạp chí Cell, hệ thống hóa toàn bộ lĩnh vực. Họ xác định chín — nay đã cập nhật thành mười hai — Dấu Ấn Lão Hóa (Hallmarks of Aging):
- Bất ổn định bộ gene (Genomic instability)
- Mòn ngắn telomere (Telomere attrition)
- Biến đổi biểu sinh (Epigenetic alterations)
- Mất cân bằng protein (Loss of proteostasis)
- Suy giảm tự thực bào (Disabled macroautophagy)
- Rối loạn cảm nhận dinh dưỡng (Deregulated nutrient-sensing)
- Rối loạn chức năng ty thể (Mitochondrial dysfunction)
- Lão hóa tế bào (Cellular senescence)
- Cạn kiệt tế bào gốc (Stem cell exhaustion)
- Biến đổi giao tiếp gian bào (Altered intercellular communication)
- Viêm mạn tính (Chronic inflammation)
- Loạn khuẩn (Dysbiosis)
Khung lý thuyết này mang lại cho toàn lĩnh vực một ngôn ngữ chung. Mọi can thiệp — từ senolytics đến bổ sung NAD+ hay rapamycin — giờ đây đều có thể được ánh xạ đến các dấu ấn cụ thể. Lão hóa không còn là bí ẩn mơ hồ. Nó là một bài toán kỹ thuật với các mục tiêu xác định.
Điều Này Có Ý Nghĩa Gì Với Bạn
Bạn không cần chờ đợi một loại thuốc thần kỳ duy nhất. Khung Dấu Ấn Lão Hóa cho thấy lão hóa là quá trình đa nguyên nhân — và các chiến lược mạnh mẽ nhất tác động đồng thời lên nhiều dấu ấn. Dinh dưỡng, vận động, giấc ngủ và bổ sung có chủ đích có thể nhắm trúng sáu dấu ấn trở lên cùng lúc.
Câu hỏi không còn là liệu lão hóa có thể bị làm chậm. Mà là bạn sẵn sàng hành động quyết liệt đến đâu dựa trên những gì khoa học đã chứng minh.
Điểm Mấu Chốt
- Thí nghiệm năm 2011 của Jan van Deursen tại Mayo Clinic chứng minh rằng loại bỏ tế bào lão hóa có thể đảo ngược suy thoái do tuổi tác và kéo dài tuổi thọ 25–35% ở chuột
- Ba bước đột phá hội tụ — senolytics, phục hồi NAD+, và kích hoạt sirtuin — tạo thành nền tảng của khoa học trường thọ hiện đại
- Khung Dấu Ấn Lão Hóa đã biến lão hóa từ một bí ẩn nan giải thành bài toán kỹ thuật đa con đường, có mục tiêu rõ ràng — và bạn có thể bắt đầu can thiệp ngay hôm nay

Tế Bào Lão Hóa: Cuộc Khủng Hoảng Zombie Ngay Bên Trong Bạn
Chúng không chết. Chúng không phân chia. Và chúng không chịu rời đi trong im lặng.
Tế bào lão hóa (senescent cells) là những tế bào vốn từng khỏe mạnh nhưng đã chịu tổn thương không thể phục hồi — do đứt gãy DNA, bào mòn telomere, stress oxy hóa, hoặc tín hiệu sinh ung. Thay vì làm điều mà tế bào hư hỏng lẽ ra phải làm (tự hủy thông qua quá trình apoptosis), chúng bước vào trạng thái ngừng hoạt động vĩnh viễn. Chúng ngưng thực hiện chức năng. Nhưng chúng từ chối chết đi.
Và chính sự từ chối ấy đang âm thầm đầu độc bạn từ bên trong.
Sinh Học Của Một Tế Bào “Xác Sống”
Trong điều kiện bình thường, lão hóa tế bào thực chất là một cơ chế bảo vệ. Khi DNA của tế bào bị tổn thương quá nặng để có thể nhân đôi an toàn, quá trình lão hóa tế bào đóng vai trò như một phanh khẩn cấp — chặn đứng sự phân chia để ngăn tế bào đó trở thành ung thư.
Khi còn trẻ, hệ miễn dịch của bạn nhận diện và loại bỏ những tế bào bị bắt giữ này một cách hiệu quả. Tế bào diệt tự nhiên (NK cells) và đại thực bào (macrophages) tuần tra khắp các mô, đánh dấu tế bào lão hóa để loại bỏ và xử lý chúng trong vòng vài ngày.
Hệ thống này vận hành hoàn hảo — khi bạn 25 tuổi.
Nhưng khi chức năng miễn dịch suy giảm theo tuổi — một quá trình gọi là suy lão hóa miễn dịch (immunosenescence) — tốc độ thanh thải chậm lại. Tế bào lão hóa bắt đầu tích tụ. Chúng cắm rễ trong các mô của bạn như những kẻ chiếm dụng không chịu bị trục xuất. Và rồi chúng bắt đầu làm điều còn tồi tệ hơn nhiều so với việc chỉ chiếm chỗ.
Chúng bắt đầu “phát tín hiệu.”
SASP: Tín Hiệu Phát Sóng Độc Hại
Vào năm 1999, nhà sinh học tế bào Judith Campisi tại Viện Buck Institute for Research on Aging đã đưa ra một phát hiện làm thay đổi hoàn toàn cách chúng ta hiểu về quá trình suy thoái của cơ thể.
Bà phát hiện rằng tế bào lão hóa không nằm yên lặng lẽ. Chúng chủ động tiết ra một hỗn hợp phân tử viêm có sức tàn phá khủng khiếp — một hiện tượng bà đặt tên là Senescence-Associated Secretory Phenotype, hay SASP.
💡 Quick Fact: Chỉ một tế bào lão hóa duy nhất có thể tiết ra hơn 40 loại cytokine tiền viêm, chemokine, yếu tố tăng trưởng và protease khác nhau — liên tục, suốt nhiều năm.
SASP bao gồm một số phân tử có sức hủy diệt mạnh nhất trong sinh học người:
- IL-6 và IL-1β — các cytokine viêm chủ đạo thúc đẩy tình trạng viêm mạn tính toàn thân
- TNF-α — yếu tố hoại tử khối u liên quan đến kháng insulin, teo cơ và thoái hóa thần kinh
- MMP-3 và MMP-9 — các matrix metalloproteinase phá hủy vật lý cấu trúc mô xung quanh tế bào lão hóa
- VEGF — yếu tố tăng trưởng thúc đẩy hình thành mạch máu bất thường, tiếp nhiên liệu cho sự phát triển khối u
- MCP-1 — chemokine thu hút tế bào miễn dịch, khuếch đại viêm cục bộ thành khủng hoảng viêm lan rộng toàn mô
Đây là điều khiến SASP thực sự nguy hiểm. SASP không chỉ phá hủy mô xung quanh. Nó biến các tế bào khỏe mạnh lân cận thành tế bào lão hóa.
Nghiên cứu của Campisi đã chứng minh hiệu ứng bàng quan (bystander effect) này — một tế bào xác sống duy nhất có thể kích hoạt chuỗi phản ứng lão hóa lan truyền sang các tế bào xung quanh. Một trở thành mười. Mười trở thành hàng trăm. Đó là một sự lây lan sinh học đang diễn ra ngay bên trong cơ thể bạn.
Điều Này Có Ý Nghĩa Gì Với Bạn
Mỗi tế bào lão hóa trong cơ thể bạn là một nhà máy viêm thu nhỏ hoạt động 24 giờ mỗi ngày, 7 ngày mỗi tuần. SASP hiện được công nhận là một trong những động lực chính của inflammaging — tình trạng viêm mạn tính cấp độ thấp nằm dưới hầu hết mọi bệnh lý liên quan đến tuổi tác. Ức chế hoặc loại bỏ những tế bào này không chỉ làm chậm lão hóa. Nó loại bỏ một trong những nguyên nhân gốc rễ của lão hóa.
Đường Cong Tích Lũy: Từ 2% Lên 15%
Ở độ tuổi hai mươi và ba mươi, tế bào lão hóa chiếm khoảng 1-2% tổng số tế bào của bạn. Hệ miễn dịch vẫn theo kịp. Tổn thương được sửa chữa hoặc loại bỏ. Chức năng mô vẫn duy trì ở mức cao.
Đến tuổi bốn mươi, khả năng thanh thải bắt đầu tụt hậu. Gánh nặng tế bào lão hóa leo lên 4-6%. Bạn có thể chưa cảm nhận được — nhưng các chỉ dấu viêm đang tăng, sửa chữa mô đang chậm lại, và dự trữ chức năng tạng đang âm thầm suy giảm.
Đến tuổi 60-70, tế bào lão hóa có thể chiếm 10-15% tổng số tế bào trong các mô bị ảnh hưởng. Ở nồng độ này, sản lượng SASP đạt đến điểm bùng phát. Cấu trúc mô bắt đầu sụp đổ cả về hình thái lẫn chức năng.
Các cơ quan bị tổn thương nặng nhất lại chính là những cơ quan bạn không thể thiếu:
- Da — nguyên bào sợi lão hóa phân hủy collagen và elastin, gây nhăn nheo, mỏng da và suy giảm khả năng lành vết thương
- Thận — tế bào ống thận lão hóa đẩy nhanh quá trình mất nephron; chức năng thận có thể suy giảm 30-40% vào tuổi 70
- Phổi — tế bào phế nang lão hóa giảm hiệu quả trao đổi khí và thúc đẩy xơ phổi
- Gan — tế bào gan lão hóa suy giảm khả năng giải độc, chuyển hóa lipid và năng lực tái tạo
- Khớp — tế bào sụn lão hóa (chondrocytes) trong sụn khớp là yếu tố thúc đẩy chính của thoái hóa khớp, phá hủy mô từ bên trong
- Hệ mạch — tế bào nội mô lão hóa làm cứng thành động mạch, thúc đẩy hình thành mảng xơ vữa và tăng nguy cơ tim mạch
- Não — tế bào hình sao (astrocytes) và vi thần kinh đệm (microglia) lão hóa khuếch đại tình trạng viêm thần kinh, hiện được liên kết với bệnh Alzheimer, Parkinson và suy giảm nhận thức
💡 Quick Fact: Trong một nghiên cứu mang tính bước ngoặt năm 2018 công bố trên Nature Medicine, các nhà nghiên cứu tại Mayo Clinic chứng minh rằng chỉ cần cấy ghép một số lượng nhỏ tế bào lão hóa vào chuột trẻ đã gây ra suy giảm chức năng thể chất kéo dài, giảm tỷ lệ sống sót và đẩy nhanh lão hóa sinh học — chứng minh rằng tế bào lão hóa đơn độc cũng đủ để gây ra các kiểu hình lão hóa.
Đo Lường Gánh Nặng Tế Bào Lão Hóa Của Bạn
Bạn không thể quản lý thứ bạn không đo lường được. Cho đến gần đây, việc định lượng tải lượng tế bào lão hóa đòi hỏi sinh thiết mô — không thực tế cho theo dõi định kỳ. Điều này đang thay đổi nhanh chóng.
Các phương pháp đo lường hiện tại và đang phát triển bao gồm:
- Biểu hiện p16^INK4a (xét nghiệm máu) — p16 là chỉ dấu sinh học được xác nhận rộng rãi nhất về lão hóa tế bào; nồng độ tăng trong tế bào T tuần hoàn tương quan chặt chẽ với tuổi sinh học và gánh nặng tế bào lão hóa
- Protein phản ứng C siêu nhạy (hsCRP) — tuy không đặc hiệu cho lão hóa tế bào, hsCRP tăng phản ánh sản lượng viêm toàn thân từ SASP; mức tối ưu dưới 0,5 mg/L, nhưng hầu hết người trưởng thành trên 50 tuổi đo được 2,0-4,0 mg/L
- Bảng xét nghiệm IL-6 và TNF-α — đo trực tiếp các cytokine SASP chủ chốt; các bảng xét nghiệm viêm nâng cao này có sẵn tại các phòng xét nghiệm y học chức năng
- Xét nghiệm GlycanAge — đo các mô hình glycan trên immunoglobulin G thay đổi theo gánh nặng viêm và lão hóa tế bào, cung cấp chỉ số gián tiếp về lão hóa miễn dịch
- Hoạt tính SA-β-galactosidase — tiêu chuẩn vàng trong nghiên cứu; phát hiện hoạt tính enzyme liên quan đến lão hóa tế bào trong mẫu mô
- Đồng hồ biểu sinh (GrimAge, DunedinPACE) — tuy không đặc hiệu cho lão hóa tế bào, các đồng hồ này nắm bắt quá trình lão hóa sinh học hạ nguồn do tích tụ tế bào lão hóa và phơi nhiễm SASP
Điều Này Có Ý Nghĩa Gì Với Bạn
Bạn không cần phòng thí nghiệm nghiên cứu để bắt đầu theo dõi. Sự kết hợp giữa hsCRP, IL-6 và xét nghiệm đồng hồ biểu sinh cho bạn bức tranh thực tế, có thể hành động ngay về gánh nặng viêm và tế bào lão hóa hiện tại. Xét nghiệm hàng năm. Theo dõi xu hướng.
“Lão hóa không đơn thuần là thời gian trôi qua. Đó là sự mất mát thông tin biểu sinh (epigenetic). Và những gì đã mất, ít nhất một phần, có thể được phục hồi.”
Senolytics: Khoa Học Tiêu Diệt Tế Bào Zombie
Suốt nhiều thập kỷ, y học không có câu trả lời cho hiện tượng lão hóa tế bào (cellular senescence). Chúng ta có thể làm chậm nó. Có thể đo lường nó. Nhưng không thể loại bỏ chọn lọc những tế bào đang thúc đẩy quá trình này.
Điều đó đã thay đổi vào năm 2015. Và đây có thể là bước đột phá quan trọng nhất trong khoa học trường thọ của thế kỷ này.
Senolytics là một nhóm hợp chất mới được thiết kế để thực hiện duy nhất một nhiệm vụ: tìm ra tế bào lão hóa và tiêu diệt chúng — trong khi giữ nguyên các tế bào khỏe mạnh. Không phải làm chậm lão hóa. Không phải kiểm soát triệu chứng. Mà loại bỏ tận gốc nguồn gây bệnh.
Lĩnh vực này đã tiến từ đĩa nuôi cấy đến thử nghiệm lâm sàng trên người chỉ trong chưa đầy một thập kỷ. Dưới đây là bức tranh toàn cảnh khoa học tại thời điểm hiện tại.
Bước Đột Phá: Dasatinib + Quercetin (D+Q)
Câu chuyện bắt đầu tại Mayo Clinic với TS. James Kirkland và TS. Tamara Tchkonia.
Phát hiện của họ vô cùng tinh tế. Tế bào lão hóa sống sót được là nhờ kích hoạt tăng cường các con đường chống chết theo chương trình (anti-apoptotic pathways) — về bản chất, đó là những lá chắn phân tử ngăn không cho chúng trải qua quá trình chết tế bào theo chương trình. Chúng đã hư hỏng đến mức không thể sửa chữa, nhưng lại “hack” được chính cơ chế tự hủy của mình.
Nhóm của Kirkland đặt ra một câu hỏi đơn giản: Nếu chúng ta vô hiệu hóa những lá chắn đó thì sao?
Họ sàng lọc hàng chục hợp chất và tìm ra một tổ hợp mạnh mẽ:
- Dasatinib — một thuốc điều trị ung thư ức chế tyrosine kinases và tín hiệu thụ thể ephrin, nhắm vào tế bào tiền thân mô mỡ và hệ mạch máu đã lão hóa
- Quercetin — một flavonoid thực vật ức chế nhóm protein BCL-2, PI3K và serpine, nhắm vào tế bào nội mô và tế bào gốc tủy xương đã lão hóa
Dùng riêng lẻ, mỗi hợp chất có hiệu quả ở mức trung bình. Kết hợp lại, chúng có sức hủy diệt mạnh mẽ — quét sạch tế bào lão hóa đồng thời trên nhiều loại mô khác nhau.
💡 Quick Fact: Trong nghiên cứu mang tính bước ngoặt năm 2019 trên chuột của Kirkland, chỉ một đợt điều trị D+Q duy nhất đã kéo dài thời gian sống còn lại thêm 36% ở chuột già — tương đương với việc tăng thêm khoảng 9 năm tuổi thọ ở người chỉ từ một lần điều trị.
Từ Chuột Đến Người
Nhóm nghiên cứu Mayo hành động rất nhanh. Các kết quả chính trên người:
- Thử nghiệm thí điểm năm 2019 trên bệnh nhân xơ phổi vô căn (idiopathic pulmonary fibrosis) — một bệnh lý được thúc đẩy bởi sự tích tụ tế bào lão hóa: chỉ 3 liều trong 3 tuần đã tạo ra cải thiện đo lường được về khoảng cách đi bộ 6 phút, tốc độ đứng lên từ ghế, và giảm các biomarker SASP
- Các thử nghiệm mở rộng năm 2023 cho thấy D+Q giảm các chỉ dấu tế bào lão hóa trong mô mỡ 30-40% sau một phác đồ xung ngắn
- Các nghiên cứu đang tiến hành tại Mayo đang thử nghiệm D+Q trong bệnh Alzheimer, bệnh thận do đái tháo đường, và suy yếu liên quan đến tuổi tác (frailty) — ba tình trạng mà gánh nặng tế bào lão hóa đóng vai trò trực tiếp
Nguyên tắc thiết kế then chốt: bạn không dùng senolytics hằng ngày. Tế bào lão hóa cần hàng tuần để tích tụ trở lại. Vì vậy, phác đồ là ngắt quãng — các đợt xung ngắn, tập trung cao, xen kẽ với giai đoạn nghỉ dài.
Đây là nguồn gốc của phác đồ xung 2 ngày mỗi quý nổi tiếng hiện nay:
- Ngày 1–2: Dasatinib (100 mg/ngày) + Quercetin (1.000–1.250 mg/ngày)
- Ngày 3–90: Không dùng gì. Để cơ thể dọn dẹp mảnh vụn tế bào và tái tạo.
- Lặp lại mỗi quý — khoảng 4 đợt mỗi năm
Sự tinh tế nằm ở tính ngắn gọn. Hai ngày tiêu diệt có mục tiêu. Chín mươi ngày phục hồi và tái sinh.
Bạn không cần dùng thuốc liên tục để giải quyết gánh nặng tế bào lão hóa. Phương pháp xung đồng nghĩa với phơi nhiễm thuốc tối thiểu, tác dụng phụ tối thiểu, và hiệu quả thanh thải tối đa — một hồ sơ dược lý gần như không giống bất kỳ thứ gì khác trong y học hiện đại.
Fisetin: Senolytic Dễ Tiếp Cận
Không phải ai cũng tiếp cận được dasatinib. Và đây là lúc fisetin xuất hiện — một flavonoid tự nhiên có trong dâu tây, táo và hồng.
Các nhà nghiên cứu tại Đại học Minnesota, dẫn đầu bởi TS. Paul Robbins và TS. Laura Niedernhofer, đã chứng minh rằng fisetin:
- Giảm gánh nặng tế bào lão hóa ở chuột già khoảng 25-50% tùy loại mô
- Kéo dài tuổi thọ trung vị và tuổi thọ tối đa trong các mô hình chuột già
- Cho thấy hiệu lực đặc biệt mạnh trong việc loại bỏ tế bào lão hóa ở mô não, gan và thận
Thử nghiệm AFFIRM-LITE và các nghiên cứu liên quan tại Đại học Minnesota hiện đang đánh giá fisetin trên người cho các tình trạng liên quan đến tuổi tác. Dữ liệu sơ bộ cho thấy fisetin dung nạp tốt với hồ sơ an toàn vững chắc — yếu tố then chốt cho một hợp chất mà con người có thể sử dụng trong nhiều thập kỷ.
Liều dùng phổ biến trong cộng đồng trường thọ tuân theo cùng logic xung: khoảng 500–1.500 mg/ngày trong 2 ngày liên tiếp, lặp lại hằng tháng hoặc hằng quý. Đây chưa phải phác đồ senolytic được FDA phê duyệt — nhưng dữ liệu cơ chế và tiền lâm sàng đủ thuyết phục để nhiều bác sĩ chuyên về trường thọ đưa vào phác đồ điều trị.
💡 Quick Fact: Bạn sẽ cần ăn khoảng 17 kg dâu tây để đạt được một liều điều trị fisetin duy nhất. Bổ sung qua viên uống là bắt buộc, không có lựa chọn khác.
Biên Giới Tiếp Theo: Navitoclax, CAR-T và Senolysis Chính Xác
Kỷ nguyên D+Q và fisetin mới chỉ là thế hệ thứ nhất. Làn sóng tiếp theo nhắm mục tiêu chính xác hơn nhiều.
Navitoclax (ABT-263) là một chất ức chế BCL-2 và BCL-xL mạnh — trực tiếp vô hiệu hóa các protein chống chết mà tế bào lão hóa phụ thuộc để tồn tại. Nó cực kỳ hiệu quả nhưng kèm theo một tác dụng phụ đáng kể: giảm tiểu cầu (thrombocytopenia). Nghiên cứu hiện tại đang tập trung vào việc phát triển các hệ thống phân phối nhắm mục tiêu mô đặc hiệu để khai phóng sức mạnh của nó một cách an toàn.
Unity Biotechnology — một công ty công nghệ sinh học đồng sáng lập bởi TS. Judith Campisi, nhà tiên phong trong lĩnh vực lão hóa tế bào — đã phát triển UBX1325, một chất ức chế BCL-xL được tiêm trực tiếp vào mắt để điều trị phù hoàng điểm do đái tháo đường và suy giảm thị lực liên quan đến tuổi tác. Dữ liệu Pha 2 của họ cho thấy cải thiện có ý nghĩa về thị lực chỉ với một mũi tiêm duy nhất. Đây là senolytic nhắm mô đặc hiệu đầu tiên đang tiến gần đến ứng dụng lâm sàng.
Và tiếp đến là phương pháp tham vọng nhất.
Các nhà nghiên cứu Stanford dẫn đầu bởi TS. Corina Amor Vegas đã công bố một nghiên cứu đột phá năm 2024 trên tạp chí Nature Aging chứng minh CAR-T senolytics — các tế bào miễn dịch được lập trình lại để săn lùng và tiêu diệt tế bào lão hóa. Mục tiêu của chúng: các tế bào biểu hiện uPAR (urokinase plasminogen activator receptor), một chỉ dấu bề mặt tập trung cao trên tế bào lão hóa.
Kết quả trên chuột vô cùng ấn tượng:
- Giảm đáng kể gánh nặng tế bào lão hóa trên nhiều cơ quan
- Cải thiện chức năng chuyển hóa, bao gồm dung nạp glucose tốt hơn
- Một lần truyền duy nhất tạo ra hiệu quả thanh thải bền vững kéo dài nhiều tháng — tiềm năng trở thành liệu pháp senolytic một lần duy nhất là đủ
Đây là tương lai: thuốc sống tuần tra trong cơ thể bạn, tiêu diệt tế bào zombie ngay khoảnh khắc chúng xuất hiện.
Tiếp Cận Ngay Hôm Nay: AgelessRx và Các Phác Đồ Lâm Sàng
Đối với những ai muốn sử dụng senolytics ngay bây giờ, AgelessRx — một phòng khám trường thọ từ xa (telehealth) — là một trong những đơn vị đầu tiên cung cấp phác đồ D+Q và fisetin có giám sát y khoa cho bệnh nhân, đồng thời đóng góp vào các nghiên cứu lâm sàng như thử nghiệm PEARL (Participatory Evaluation of Aging with Rapamycin for Longevity).
Mô hình của họ đại diện cho một bước ch

NAD+: Phân Tử Năng Lượng Chủ Chốt Của Tế Bào Bạn Đang Cạn Kiệt
Mỗi giây trong đời bạn, các tế bào thực hiện hàng ngàn phản ứng sinh hóa. Chúng sửa chữa DNA. Chúng sản xuất năng lượng. Chúng giao tiếp, phân chia và phòng vệ.
Hầu như không phản ứng nào diễn ra mà thiếu NAD+.
Nicotinamide adenine dinucleotide — NAD+ — là một coenzyme hiện diện trong mọi tế bào sống. Nó không phải thứ tùy chọn. Không phải dưỡng chất xa xỉ. Nó, không hề phóng đại, là một trong những phân tử thiết yếu nhất duy trì sự sống của con người.
Và bạn đang mất dần nó. Ngay lúc này. Đều đặn. Âm thầm.
Sự Suy Giảm Chưa Ai Nói Cho Bạn Biết
Đến khi bạn 50 tuổi, nồng độ NAD+ đã giảm khoảng 50% so với lúc hai mươi. Đến 70 tuổi, một số mô chỉ còn giữ lại 10–25% lượng NAD+ thời trẻ.
Đây không phải sụt giảm nhẹ. Đây là sụp đổ.
💡 Quick Fact: Một nghiên cứu mang tính bước ngoặt năm 2015 trên Cell Metabolism phát hiện rằng sự suy giảm NAD+ theo tuổi được bảo tồn xuyên loài — từ giun đến chuột đến người — cho thấy đây là một cơ chế thúc đẩy lão hóa sinh học mang tính nền tảng và phổ quát.
Khi NAD+ sụt giảm, mọi thứ hạ nguồn đều sụt theo:
- Sản xuất năng lượng ty thể — tế bào tạo ra ít ATP hơn, khiến bạn mệt mỏi ở cấp độ tế bào
- Sửa chữa DNA — các đoạn đứt gãy tích lũy nhanh hơn khả năng phục hồi của cơ thể
- Kích hoạt sirtuin — các enzyme liên quan đến trường thọ SIRT1–SIRT7 cần NAD+ làm nhiên liệu; thiếu nó, chúng ngừng hoạt động
- Điều hòa nhịp sinh học — dao động NAD+ chi phối đồng hồ sinh học nội tại; sự cạn kiệt phá vỡ cấu trúc giấc ngủ
- Khả năng chống chịu stress tế bào — năng lực xử lý tổn thương oxy hóa, sốc nhiệt và độc tố suy giảm rõ rệt
Sự suy giảm NAD+ không chỉ tương quan với lão hóa. Theo GS. David Sinclair, nhà di truyền học tại Harvard, nó có thể gây ra phần lớn những gì chúng ta trải nghiệm là lão hóa.
Tại Sao Bạn Đang Mất NAD+: Ba Cơ Chế Tiêu Hao Ở Cấp Phân Tử
NAD+ không tự bốc hơi. Ba quá trình sinh học cụ thể chủ động tiêu hao và ức chế nó khi bạn lão hóa.
1. Tăng hoạt quá mức PARP
PARPs (poly ADP-ribose polymerases) là các enzyme chịu trách nhiệm sửa chữa DNA. Mỗi khi một sợi DNA đứt gãy — do tia UV, stress oxy hóa, hoặc hao mòn chuyển hóa thông thường — PARPs lập tức được huy động và tiêu thụ NAD+ làm nhiên liệu sửa chữa.
Vấn đề là gì? Tổn thương DNA tích lũy theo tuổi. Tổn thương nhiều hơn nghĩa là hoạt tính PARP cao hơn, nghĩa là NAD+ bị tiêu hao nhiều hơn. Nó trở thành một vòng xoáy luẩn quẩn — phân tử bạn cần nhất lại bị đốt cháy nhanh nhất đúng lúc gánh nặng sửa chữa ở mức cao nhất.
2. Biểu hiện quá mức CD38
CD38 là enzyme được biểu hiện chủ yếu trên tế bào miễn dịch. Khi còn trẻ, nó đóng vai trò được điều hòa trong tín hiệu canxi và chức năng miễn dịch. Nhưng theo tuổi — cùng với viêm mạn tính gia tăng — biểu hiện CD38 tăng lên đáng kể.
Tại sao điều này quan trọng:
- CD38 là một trong những tác nhân tiêu hao NAD+ mạnh nhất trong cơ thể
- Một nghiên cứu năm 2016 trên Cell Metabolism chứng minh rằng nồng độ CD38 tăng đáng kể theo tuổi và ức chế CD38 ở chuột già giúp phục hồi nồng độ NAD+ gần bằng mức trẻ tuổi
- Inflammaging thúc đẩy CD38. Bạn mang càng nhiều viêm mạn tính, NAD+ càng biến mất nhanh hơn
3. Suy giảm sinh tổng hợp
Cơ thể bạn tổng hợp NAD+ qua nhiều con đường — chủ yếu là con đường thu hồi (salvage pathway) (tái chế nicotinamide) và con đường tổng hợp de novo (từ tryptophan). Cả hai con đường đều giảm hiệu suất theo tuổi.
Các enzyme chủ chốt như NAMPT — enzyme giới hạn tốc độ trong con đường thu hồi — suy giảm hoạt tính. Kết quả: bạn tạo ra ít NAD+ hơn trong khi đồng thời đốt cháy nhiều hơn.
Khủng hoảng NAD+ là cuộc chiến trên ba mặt trận. Bạn sản xuất ít hơn, tiêu thụ nhiều hơn, và mất dần bộ máy enzyme để tái chế phần còn lại. Chiến lược bổ sung phải giải quyết cả ba mặt trận — không chỉ một.
NMN so với NR: Cuộc Tranh Luận Về Tiền Chất, Được Giải Quyết Bằng Dữ Liệu
Hai chiến lược chính để nâng NAD+ là các tiền chất: NMN (nicotinamide mononucleotide) và NR (nicotinamide riboside). Cả hai đều được chuyển hóa thành NAD+ bên trong tế bào. Nhưng chúng không giống nhau.
NMN (Nicotinamide Mononucleotide)
- Chỉ cách NAD+ một bước enzyme — tiền chất trực tiếp hơn
- Cần chất vận chuyển Slc12a8 để hấp thu trực tiếp vào tế bào, được xác định trong nghiên cứu năm 2019 trên Nature Metabolism
- Kết quả công bố năm 2024 của thử nghiệm lâm sàng Đại học Washington (do TS. Shin-ichiro Imai dẫn đầu) cho thấy 250 mg/ngày NMN cải thiện đáng kể độ nhạy insulin cơ và chuyển hóa glucose ở phụ nữ mãn kinh tiền đái tháo đường
- Một thử nghiệm ngẫu nhiên có đối chứng năm 2023 công bố trên GeroScience chứng minh bổ sung NMN liều 600–1200 mg/ngày giảm các chỉ dấu tuổi sinh học và cải thiện khoảng cách đi bộ 6 phút ở người trung niên trong vòng 60 ngày
NR (Nicotinamide Riboside)
- Cần hai bước chuyển hóa enzyme để thành NAD+ — con đường dài hơn một chút
- Tiền chất được nghiên cứu thương mại nhiều nhất, chủ yếu qua dòng sản phẩm ChromaDex/Niagen
- Một thử nghiệm năm 2023 công bố trên Aging Cell cho thấy NR liều 1000 mg/ngày nâng NAD+ trong máu toàn phần khoảng 100% trong hai tuần — nhưng cải thiện triệu chứng lâm sàng khiêm tốn hơn
- Một số bằng chứng gợi ý NR có thể có sinh khả dụng mô thấp hơn ở liều tương đương so với NMN
Kết Luận:
- NMN dường như có lợi thế nhẹ trong dữ liệu thử nghiệm trên người gần đây về kết cục chức năng — đặc biệt ở liều 500–1000 mg/ngày
- NR vẫn là lựa chọn hợp lệ, nhất là ở liều cao hơn, với hồ sơ an toàn dài hạn hơn
- Không có tiền chất nào là viên đạn thần kỳ đơn lẻ — cả hai hoạt động tốt nhất trong một phác đồ phục hồi NAD+ toàn diện
NAD+ Đường Tĩnh Mạch: Con Đường Trực Tiếp
Đối với những ai tìm kiếm phục hồi NAD+ nhanh và mạnh, truyền tĩnh mạch NAD+ bỏ qua hoàn toàn đường tiêu hóa.
Những điều cần biết:
- Phác đồ lâm sàng điển hình sử dụng 250–750 mg truyền trong 2–4 giờ
- Người dùng thường báo cáo cải thiện tức thì về sáng suốt tinh thần, năng lượng và tâm trạng — dù các ghi nhận chủ quan này vượt trước dữ liệu lâm sàng đã công bố
- Một nghiên cứu thí điểm năm 2023 trên Journal of Translational Medicine xác nhận NAD+ đường tĩnh mạch nâng nhanh và đáng kể nồng độ NAD+ huyết tương — cao hơn đáng kể so với tiền chất đường uống
- Truyền có thể gây khó chịu — buồn nôn, tức ngực và chuột rút thường gặp trong quá trình truyền
NAD+ đường tĩnh mạch phù hợp nhất như chiến lược nạp tải — một cú tăng cường ban đầu để khôi phục dự trữ cạn kiệt — sau đó duy trì bằng phác đồ tiền chất đường uống.
Apigenin: Chất Ức Chế CD38 Ẩn Ngay Trước Mắt
Còn nhớ cơ chế tiêu hao thứ hai — biểu hiện quá mức CD38? Có một hợp chất tự nhiên ức chế nó.
Apigenin là một flavonoid có trong:
- Trà hoa cúc (chamomile) (nguồn thực phẩm giàu nhất)
- Rau mùi tây
- Cần tây
- Lá oregano khô
Một nghiên cứu năm 2015 công bố trên Journal of Biological Chemistry chứng minh apigenin là chất ức chế CD38 mạnh và đặc hiệu — làm chậm sự phân hủy NAD+ thay vì tăng sản xuất.
Đây là điểm khác biệt then chốt. Apigenin không thêm nhiên liệu. Nó bịt lỗ rò.
Ở liều bổ sung 250–500 mg/ngày, apigenin kết hợp mạnh mẽ với NMN hoặc NR — một bên thúc đẩy sản xuất trong khi bên kia giảm phân hủy.
💡 Quick Fact: Kết hợp tiền chất NAD+ với chất ức chế CD38 như apigenin có thể hiệu quả hơn việc tăng gấp đôi liều tiền chất đơn thuần, theo mô hình tiền lâm sàng từ Buck Institute for Research on Aging.
Chiến lược NAD+ t

Sirtuins: Các Gen Trường Thọ Được NAD+ Đánh Thức
NAD+ không chỉ cung cấp năng lượng cho tế bào. Nó kích hoạt một họ protein cổ xưa — có thể là nhóm chất điều hòa trường thọ quan trọng nhất từng được phát hiện.
Chúng được gọi là sirtuins. Và khi thiếu NAD+, chúng nằm im bất hoạt — như những công tắc tổng bị khóa vĩnh viễn ở vị trí tắt.
Khám Phá Tại MIT Mở Ra Cả Một Lĩnh Vực Nghiên Cứu
Năm 1999, nhà sinh học phân tử GS. Leonard Guarente tại MIT công bố một phát hiện làm thay đổi toàn bộ khoa học lão hóa trong suốt một phần tư thế kỷ tiếp theo.
Phòng thí nghiệm của ông phát hiện rằng một gen tên SIR2 — sau này được đổi tên thành SIRT1 ở động vật có vú — có khả năng kéo dài đáng kể tuổi thọ của nấm men. Nhưng chỉ khi gen này tiếp cận được lượng NAD+ đủ ngưỡng. Không có NAD+, không có hoạt hóa. Không có hoạt hóa, không có lợi ích trường thọ.
Đây là một bước ngoặt về mặt nhận thức khoa học. Nó cho thấy lão hóa không đơn thuần là quá trình entropy thụ động — mà một phần là quá trình được điều hòa chủ động, chi phối bởi các enzyme cảm nhận dinh dưỡng có thể bật hoặc tắt tùy thuộc vào điều kiện chuyển hóa.
Công trình của Guarente hé lộ những điều phi thường:
- Sirtuins là các deacetylase phụ thuộc NAD+ — chúng loại bỏ nhóm acetyl khỏi protein để thay đổi chức năng của protein đó
- Chúng tiến hóa như các cảm biến phản ứng stress — được kích hoạt khi hạn chế calo, nhịn ăn gián đoạn và các thử thách chuyển hóa
- Động vật có vú có bảy sirtuin (SIRT1–SIRT7) — mỗi loại hoạt động tại các khoang tế bào khác nhau với vai trò riêng biệt nhưng có phần chồng lấn
💡 Quick Fact: Khám phá ban đầu về SIR2 của Guarente cho thấy tuổi thọ nấm men tăng 30% — một trong những hiệu ứng đơn gen lớn nhất lên tuổi thọ từng được ghi nhận tại thời điểm đó.
Hàm ý của phát hiện này vô cùng sâu rộng. NAD+ không chỉ là nhiên liệu tế bào. Nó là chìa khóa kích hoạt cho cả một họ protein chi phối tuổi thọ.
Ba Sirtuin Quan Trọng Nhất
Trong bảy sirtuin ở động vật có vú, ba loại nổi lên là quan trọng nhất đối với tuổi thọ khỏe mạnh (healthspan) và tổng tuổi thọ (lifespan) ở người. Mỗi loại hoạt động tại một vị trí tế bào khác nhau. Cùng nhau, chúng tạo thành một mạng lưới phòng thủ tích hợp.
SIRT1 — Người Bảo Vệ Nhân Tế Bào
SIRT1 là sirtuin được nghiên cứu nhiều nhất, hoạt động chủ yếu trong nhân tế bào. Các chức năng của nó đọc lên như một danh sách ước mơ trường thọ:
- Kích hoạt các con đường sửa chữa DNA — huy động enzyme đến các vị trí tổn thương bộ gen
- Ức chế tín hiệu NF-κB — công tắc tổng của phản ứng viêm, tác nhân chính gây viêm mạn tính liên quan tuổi tác (inflammaging)
- Tăng cường sinh tổng hợp ty thể thông qua kích hoạt PGC-1α — theo nghĩa đen là xây dựng các nhà máy năng lượng tế bào mới
- Cải thiện độ nhạy insulin — bảo vệ chống lại rối loạn chuyển hóa và đái tháo đường típ 2
- Điều hòa các gen nhịp sinh học — duy trì đồng hồ sinh học vốn bị suy giảm theo tuổi
SIRT3 — Người Bảo Vệ Ty Thể
SIRT3 cư trú bên trong ty thể — các bào quan sản xuất năng lượng của tế bào. Các vai trò chính:
- Khử độc các gốc oxy phản ứng (ROS) bằng cách kích hoạt SOD2 — chất chống oxy hóa chủ lực của ty thể
- Tối ưu hóa quá trình oxy hóa axit béo — cải thiện tính linh hoạt chuyển hóa
- Ngăn ngừa tăng tính thấm màng ty thể — một yếu tố kích hoạt chủ chốt của quá trình chết tế bào theo chương trình (apoptosis)
- Suy giảm mạnh theo tuổi — tương quan trực tiếp với rối loạn chức năng ty thể
SIRT6 — Người Bảo Toàn Ổn Định Bộ Gen
SIRT6 có thể là sirtuin bị đánh giá thấp nhất. Nó hoạt động ở cấp độ chromatin, duy trì tính toàn vẹn cấu trúc của bộ gen:
- Sửa chữa đứt gãy DNA sợi đôi — dạng tổn thương bộ gen nguy hiểm nhất
- Ức chế các retrotransposon LINE-1 — những yếu tố di truyền “nổi loạn” tái hoạt hóa theo tuổi và thúc đẩy viêm
- Điều hòa duy trì telomere — bảo vệ đầu mút nhiễm sắc thể khỏi bị thoái hóa
- Một nghiên cứu bước ngoặt năm 2012 trên Nature cho thấy chuột đực biểu hiện quá mức SIRT6 sống thọ hơn 15,8% — một trong số ít can thiệp đơn gen kéo dài tuổi thọ ở động vật có vú
Ý Nghĩa Đối Với Bạn
Mỗi khi bạn phục hồi nồng độ NAD+ — thông qua NMN, nhịn ăn gián đoạn, hoặc tập luyện — bạn không chỉ nạp lại nhiên liệu cho tế bào. Bạn đang tái kích hoạt đồng thời SIRT1, SIRT3 và SIRT6. Đây chính là cơ chế đằng sau hầu hết các lợi ích hạ nguồn của NAD+. Nếu thiếu sirtuins, việc bổ sung NAD+ mất đi phần lớn ý nghĩa chức năng.
Lý Thuyết Thông Tin Về Lão Hóa Của Sinclair
GS. David Sinclair, cựu nghiên cứu sinh tiến sĩ của Guarente tại MIT và hiện là giáo sư di truyền học tại Harvard Medical School, đã phát triển nền tảng sirtuin để đề xuất một trong những lý thuyết thống nhất về lão hóa hấp dẫn nhất.
Ông gọi đó là Lý Thuyết Thông Tin Về Lão Hóa (Information Theory of Aging).
Luận điểm cốt lõi rất tinh gọn. DNA là phần cứng. Biểu sinh (epigenome) — hệ thống các dấu ấn hóa học chỉ dẫn mỗi tế bào biểu hiện gen nào — là phần mềm. Lão hóa, theo Sinclair, không chủ yếu do đột biến phần cứng. Mà do hỏng phần mềm.
Cơ chế diễn ra như sau:
- Tổn thương DNA xảy ra liên tục — do stress oxy hóa, bức xạ, lỗi sao chép, và các độc tố môi trường
- Sirtuins bị kéo khỏi nhiệm vụ điều hòa gen thường trực để đi sửa chữa các tổn thương này
- Mỗi lần chúng rời vị trí, thông tin biểu sinh bị mất — tế bào bắt đầu quên mình thuộc loại tế bào nào
- Qua nhiều thập kỷ, hiện tượng này tạo ra nhiễu biểu sinh (epigenetic noise) — tương đương với một đĩa CD bị trầy xước, ngày càng nhảy đoạn nhiều hơn
Bài báo năm 2023 trên Cell của Sinclair cung cấp bằng chứng ấn tượng. Nhóm nghiên cứu sử dụng hệ thống ICE (Inducible Changes to the Epigenome) để tăng tốc nhiễu biểu sinh ở chuột mà không gây đột biến DNA. Kết quả: chuột lão hóa nhanh chóng — xuất hiện lông bạc, suy giảm cơ quan, suy kiệt thể chất, và suy giảm nhận thức — chỉ từ rối loạn biểu sinh đơn thuần.
Sau đó là phần đảo ngược. Sử dụng các yếu tố Yamanaka (OSK) để tái lập trình biểu sinh, nhóm nghiên cứu phục hồi các kiểu biểu hiện gen trẻ trung và đảo ngược các chỉ dấu sinh học lão hóa.
Kết luận rất trực diện. Lão hóa, ít nhất một phần đáng kể, là vấn đề mất thông tin. Và sirtuins là đội bảo trì đang cố gắng bảo toàn thông tin đó — nhưng chỉ khi NAD+ sẵn có để cung cấp năng lượng cho chúng.
Cuộc Tranh Cãi Về Resveratrol — Đã Được Giải Quyết
Không thể thảo luận về sirtuins mà bỏ qua resveratrol — hợp chất từ rượu vang đỏ đã trở thành phân tử trường thọ nổi tiếng nhất thế giới vào giữa thập niên 2000.
Câu chuyện bắt đầu với bài báo năm 2003 trên Nature của Sinclair, cho thấy resveratrol kích hoạt SIRT1 và kéo dài tuổi thọ nấm men 70%. Cơn sốt truyền thông bùng nổ ngay lập tức. Doanh số rượu vang đỏ tăng vọt. Các công ty thực phẩm chức năng nở rộ.
Rồi làn sóng phản bác ập đến.
Một nghiên cứu năm 2010 của các nhà nghiên cứu Pfizer trên Journal of Biological Chemistry lập luận rằng khả năng hoạt hóa SIRT1 của resveratrol chỉ là sản phẩm giả (artifact) của phương pháp phân tích huỳnh quang được sử dụng — không phải hiệu ứng sinh học thực sự. Giới thực phẩm chức năng chấn động. Các tít báo tuyên bố resveratrol đã chết.
Nhưng lời giải đáp tinh tế hơn cả hai phe thừa nhận:
- Phòng thí nghiệm của Sinclair đáp trả năm 2013 trên Science, chứng minh rằng resveratrol thực sự kích hoạt SIRT1 — nhưng thông qua cơ chế dị lập thể (allosteric) đòi hỏi các điều kiện cơ chất đặc hiệu mà phân tích của Pfizer không tái lập được
- Bằng chứng in vivo vẫn nhất quán — chuột được cho ăn resveratrol kết hợp chế độ ăn giàu chất béo cho thấy cải thiện hồ sơ chuyển hóa, giảm viêm, và kéo dài tuổi thọ khỏe mạnh
- Vấn đề thực sự nằm ở sinh khả dụng, không

Quy Trình Trẻ Hóa Tế Bào Toàn Diện
Bạn đã nắm được nền tảng khoa học — sirtuin, suy giảm NAD+, trôi dạt biểu sinh, tích lũy tế bào lão hóa, suy thoái ty thể.
Câu hỏi không còn là tại sao bạn lão hóa. Mà là bạn sẽ làm gì, và theo trình tự nào.
Đây là phác đồ ba tầng của McKaizer. Mỗi tầng được xây dựng trên nền tảng của tầng trước đó. Bắt đầu từ Tầng 1. Thành thạo nó. Sau đó mới nâng tầng. Bỏ qua nền tảng để chạy theo các can thiệp tiên phong là sai lầm phổ biến nhất trong y học trường thọ.
Tầng 1 — Nền Tảng Không Thể Bỏ Qua
Đây là nơi tạo ra 80% kết quả của bạn. Mọi hợp chất, mọi thiết bị, mọi liệu pháp tương lai đều hoạt động hiệu quả hơn — hoặc chỉ có thể phát huy tác dụng — khi sáu trụ cột này đã được thiết lập.
1. NMN — 500–1.000 mg/ngày, uống vào buổi sáng cùng nguồn chất béo
- Phục hồi nồng độ NAD+ vốn suy giảm khoảng 50% từ tuổi 30 đến 60
- Cung cấp nhiên liệu cho quá trình kích hoạt sirtuin, sửa chữa DNA và sinh tổng hợp ty thể
- Bài tổng quan phân tích trên Nature Aging năm 2024 đã xác nhận khả năng bổ sung NAD+ phụ thuộc liều ở người qua 11 thử nghiệm lâm sàng
2. Trans-Resveratrol — 250–500 mg/ngày, uống cùng NMN và bữa ăn có chất béo
- Hoạt động như chất kích hoạt dị lập thể trực tiếp của SIRT1 — nó vặn chìa khóa mà NAD+ cung cấp năng lượng
- Tăng cường chức năng nội mô, giảm LDL bị oxy hóa và cải thiện độ nhạy insulin
- Bắt buộc sử dụng dạng vi hạt hóa hoặc liposome — resveratrol thông thường chỉ có sinh khả dụng khoảng 1%
3. Spermidine — 5–15 mg/ngày hoặc lượng tương đương từ thực phẩm
- Là chất kích hoạt tự thực bào tự nhiên mạnh nhất được xác định cho đến nay
- Nghiên cứu Bruneck (2018, American Journal of Clinical Nutrition) cho thấy lượng spermidine nạp vào cao tương quan với giảm 5,7 năm tử vong
- Nguồn thực phẩm: phô mai lên men lâu năm, mầm lúa mì, natto, nấm, đậu Hà Lan
Phác Đồ Vận Động
4. Cardio Vùng 2 — 150–180 phút mỗi tuần
- Đây là cường độ mà bạn có thể duy trì hội thoại nhưng không muốn nói nhiều
- Tăng mật độ ty thể, cải thiện quá trình oxy hóa chất béo và giảm viêm nền
- Bổ sung 2 buổi HIIT (20 phút mỗi buổi) để nâng VO2max — chỉ số dự báo mạnh nhất về tử vong do mọi nguyên nhân
5. Tập kháng lực — 2–3 buổi mỗi tuần
- Duy trì tổng hợp protein cơ qua con đường mTOR, vốn suy giảm khoảng 3–8% mỗi thập kỷ sau tuổi 30
- Tạo tải cơ học lên xương, gân và cân mạc — giảm nguy cơ gãy xương lên đến 40%
- Kích hoạt SIRT3 và PGC-1α trong ty thể cơ xương
6. Ăn theo khung giờ hạn chế (16:8) + Ngủ đủ 8 tiếng
- Khung nhịn ăn 16 giờ kích hoạt AMPK, ức chế mTOR và tăng cường tự thực bào
- Ngủ dưới 7 tiếng làm tăng tốc độ lão hóa biểu sinh thêm 1,5–2 năm theo Nghiên cứu Dunedin Pace of Aging (2022)
- Hai thói quen này hoàn toàn miễn phí, mang tính nền tảng và không thể thay thế
💡 Kiến thức nhanh: Chỉ riêng Tầng 1 — khi được thực hiện đầy đủ — đã tác động lên 7 trong 12 Đặc Điểm Lão Hóa theo khung lý thuyết mang tính bước ngoặt trên tạp chí Cell, cập nhật năm 2023.
Tầng 2 — Y Học Trường Thọ Có Giám Sát
Khi Tầng 1 đã được thiết lập vững chắc — thường sau 90 ngày thực hành nhất quán — bạn đã sẵn sàng cho các can thiệp có hướng dẫn y khoa, nhắm vào các cơ chế sinh học sâu hơn.
- Liệu pháp thanh thải tế bào lão hóa — Senolytics (Dasatinib + Quercetin hoặc Fisetin) — các đợt điều trị định kỳ nhằm loại bỏ tế bào lão hóa “thây ma” gây viêm mạn tính; thử nghiệm trên EBioMedicine của Mayo Clinic năm 2019 cho thấy giảm các chỉ dấu suy yếu ở người chỉ sau 3 liều
- Rapamycin liều thấp (3–6 mg/tuần, phác đồ chu kỳ) — ức chế mTOR Complex 1, tăng cường tự thực bào và tái cấu trúc miễn dịch; thử nghiệm PEARL (2023) chứng minh cải thiện chức năng miễn dịch ở người trên 65 tuổi với tác dụng phụ tối thiểu
- Metformin (500–1.500 mg/ngày) — kích hoạt AMPK, giảm sản xuất glucose từ gan và hạ thấp cytokine gây viêm; Thử nghiệm TAME (Targeting Aging with Metformin) là thử nghiệm lâm sàng đầu tiên được FDA phê duyệt với chỉ định lão hóa, dự kiến công bố kết quả 2025–2026
- Truyền tĩnh mạch NAD+ (250–500 mg, hàng tháng) — bỏ qua hấp thu qua đường tiêu hóa, đạt sinh khả dụng 100%; được sử dụng như liệu pháp “tái thiết lập” định kỳ bổ sung cho NMN đường uống hàng ngày
⚠️ Mọi can thiệp Tầng 2 đều yêu cầu xét nghiệm máu, giám sát của bác sĩ và theo dõi liên tục. Đây là những công cụ mạnh — không phải thực phẩm chức năng dùng tùy tiện.
Tầng 3 — Biên Giới Mới
Các can thiệp này đang trong giai đoạn khởi phát, mang tính thực nghiệm và chỉ khả dụng thông qua thử nghiệm lâm sàng hoặc phòng khám trường thọ chuyên biệt. Chúng đại diện cho hướng đi của khoa học — chứ chưa phải đích đến đã được xác lập.
- Thử nghiệm tái lập trình bằng Yếu tố Yamanaka — tái lập trình tế bào từng phần sử dụng các yếu tố OSK để đảo ngược tuổi biểu sinh mà không gây mất biệt hóa; Altos Labs, NewLimit và Turn Bio đang dẫn đầu các chương trình thử nghiệm trên người
- Chất đồng vận thụ thể GLP-1 (semaglutide, tirzepatide) — ngoài lợi ích chuyển hóa, dữ liệu mới cho thấy giảm viêm toàn thân, giảm 20% tử vong do tim mạch và tiềm năng bảo vệ thần kinh theo thử nghiệm SELECT (2023)
- Lọc huyết tương trị liệu (Therapeutic Plasmapheresis) — pha loãng hoặc thay thế huyết tương lão hóa nhằm giảm các yếu tố tiền lão hóa tuần hoàn; nghiên cứu năm 2020 của Giáo sư Irina Conboy tại UC Berkeley đăng trên tạp chí Aging cho thấy sự trẻ hóa mô ở chuột già chỉ bằng pha loãng huyết tương đơn thuần — thử nghiệm trên người đang được triển khai
Lộ Trình Của Bạn: Kỳ Vọng Tại Mốc 30, 90 và 365 Ngày
Tại mốc 30 ngày (Khởi động Tầng 1):
- Cải thiện chủ quan về năng lượng, cấu trúc giấc ngủ và sự minh mẫn
- Đường huyết lúc đói và cortisol buổi sáng bắt đầu có xu hướng giảm
- Thích nghi vận động — nhịp tim Vùng 2 giảm 3–5 nhịp/phút ở cùng cường độ
Tại mốc 90 ngày (Thành thạo Tầng 1 → Đủ điều kiện Tầng 2):
- Giảm đo lường được các chỉ số hsCRP, triglyceride và insulin lúc đói
- Xét nghiệm tuổi sinh học (TruAge, GrimAge) có thể cho thấy đảo ngược 1–3 năm tuổi biểu sinh
- Duy trì hoặc tăng khối lượng cơ trở nên rõ rệt; VO2max cải thiện 8–12%
Tại mốc 365 ngày (Tích hợp toàn phác đồ):
- Đảo ngược tuổi sinh học tích lũy 3–6 năm dựa trên các chuẩn lâm sàng hiện tại
- Gánh nặng tế bào lão hóa được giảm thiểu; nền viêm được tái thiết lập căn bản
- Bạn đang vận hành trên một quỹ đạo lão hóa hoàn toàn khác so với những người cùng tuổi theo lịch
💡 Kiến thức nhanh: Trong phòng thí nghiệm của Giáo sư David Sinclair, chuột được áp dụng phác đồ kết hợp NMN + vận động + hạn chế calo cho thấy mức đảo ngược tuổi sinh học tương đương hàng thập kỷ ở người — chỉ trong 8 tuần.
Điểm Mấu Chốt
- Tầng 1 chính là phác đồ — mọi thứ khác chỉ là tối ưu hóa; NMN, resveratrol, spermidine, cardio Vùng 2, tập kháng lực, nhịn ăn gián đoạn và giấc ngủ tác động lên phần lớn các đặc điểm lão hóa đã biết, với chi phí gần như không đáng kể so với y học tiên phong
- Các can thiệp Tầng 2 (senolytics, rapamycin, metformin, truyền tĩnh mạch NAD+) đều yêu cầu giám sát của bác sĩ và chỉ nên bổ sung sau 90 ngày thực hành Tầng 1 nhất quán, kèm xét nghiệm máu nền đã được thiết lập
- Kỳ vọng đảo ngược tuổi sinh học đo lường được từ 3–6 năm trong vòng 12 tháng tuân thủ toàn phác đồ — đây không phải suy đoán

Đo Tuổi Sinh Học Của Bạn: Hệ Thống Chỉ Dấu Sinh Học
Bạn không thể đảo ngược những gì bạn không đo lường được.
Đây là chân lý nền tảng của khoa học trường thọ — và cũng là lý do phần lớn mọi người thất bại. Họ uống thực phẩm bổ sung, điều chỉnh chế độ ăn, xây dựng thói quen tập luyện — rồi hy vọng rằng nó có hiệu quả. Hy vọng không phải là chỉ dấu sinh học.
Phác đồ McKaizer đòi hỏi sự chính xác. Bạn cần một hệ thống chỉ dấu sinh học — một bảng điều khiển đa tầng gồm các tín hiệu sinh học cho bạn biết, với độ chính xác lâm sàng, liệu cơ thể bạn có thực sự đang trẻ hóa hay không.
Dưới đây là cách xây dựng hệ thống này một cách chi tiết.
Tầng 1: Đồng hồ Biểu sinh — Tiêu chuẩn vàng
DNA của bạn không thay đổi theo tuổi tác. Nhưng cách DNA được đọc thì thay đổi đáng kể.
Đồng hồ biểu sinh đo lường các mẫu hình methyl hóa DNA — các dấu ấn hóa học trên hệ gen của bạn dịch chuyển theo quy luật có thể dự đoán khi bạn lão hóa. Hiện tại, đây là phương pháp đo tuổi sinh học chính xác nhất mà khoa học có được.
Hai loại đồng hồ quan trọng nhất:
- TruAge (dựa trên Horvath/GrimAge) — Được phát triển từ công trình nghiên cứu của GS. Steve Horvath tại UCLA, TruAge phân tích ~900.000 vị trí methyl hóa trên toàn bộ hệ gen của bạn. Kết quả trả về một con số duy nhất: tuổi sinh học của bạn. Xét nghiệm này còn tính toán GrimAge — chỉ số dự đoán thời gian tử vong chính xác hơn bất kỳ chỉ dấu sinh học nào đã được thẩm định hiện nay. Một lần xét nghiệm có chi phí khoảng ~300–500 USD và chỉ cần lấy máu tĩnh mạch.
- DunedinPACE — Đây là một phương pháp hoàn toàn khác biệt. Thay vì cho bạn biết sinh học của bạn bao nhiêu tuổi, nó cho bạn biết bạn đang lão hóa nhanh đến mức nào ngay lúc này. Được phát triển từ nghiên cứu dọc mang tính bước ngoặt Dunedin Longitudinal Study (theo dõi 1.037 người từ khi sinh ra), DunedinPACE trả về một điểm tốc độ. Điểm 1,0 nghĩa là bạn đang lão hóa một năm sinh học cho mỗi năm dương lịch. Dưới 1,0? Bạn đang làm chậm đồng hồ. Trên 1,0? Bạn đang tăng tốc lão hóa.
💡 Kiến thức nhanh: Trong một phân tích năm 2024 công bố trên Nature Aging, DunedinPACE là yếu tố dự đoán mạnh nhất đối với bệnh tật, khuyết tật và tử vong trong tương lai — vượt trội hơn cả tuổi thực theo năm sinh.
Điều này có ý nghĩa gì với bạn
Hãy xét nghiệm cả hai. TruAge cho bạn biết vị trí hiện tại. DunedinPACE cho bạn biết vận tốc lão hóa. Kết hợp lại, chúng tạo thành bảng đánh giá lão hóa mạnh mẽ nhất hiện có bên ngoài phòng thí nghiệm nghiên cứu.
- Thực hiện TruAge tại thời điểm ban đầu, sau 6 tháng và 12 tháng
- Thực hiện DunedinPACE song song với mỗi lần xét nghiệm TruAge để theo dõi tốc độ lão hóa
- Kỳ vọng giảm 1–3 năm tuổi sinh học mỗi khoảng sáu tháng khi tuân thủ phác đồ đầy đủ
Tầng 2: Bộ xét nghiệm Trường thọ chuyên sâu
Đồng hồ biểu sinh cho thấy bức tranh tổng thể. Các xét nghiệm chuyên sâu tiếp theo tiết lộ tại sao bạn đang lão hóa — và lĩnh vực nào cần can thiệp cấp thiết nhất.
- GlycanAge (~300 USD) — Đo lường mẫu hình glycosyl hóa immunoglobulin G, phản ánh trực tiếp tuổi viêm của hệ miễn dịch. GlycanAge đáp ứng đặc biệt tốt với các can thiệp lối sống và thường thay đổi trong vòng 90 ngày, khiến nó trở thành chỉ dấu đánh giá tiến triển lý tưởng giữa phác đồ.
- Xét nghiệm NAD+ nội bào Jinfiniti (~150 USD) — Xét nghiệm duy nhất dành cho người dùng đã được thẩm định đo nồng độ NAD+ nội bào thay vì nồng độ trong huyết tương. Điều này có ý nghĩa vô cùng lớn. NAD+ huyết tương cho bạn biết những gì đang lưu thông trong máu. Jinfiniti cho bạn biết những gì thực sự đến được tế bào của bạn. Nếu bạn đang bổ sung NMN hoặc NR mà nồng độ NAD+ nội bào không tăng, phác đồ của bạn cần được điều chỉnh.
- Xét nghiệm độ dài Telomere (ví dụ: RepeatDx, Life Length) — Đo lường các đoạn bảo vệ ở đầu nhiễm sắc thể. Tuy kém linh hoạt hơn đồng hồ methyl hóa, độ dài telomere cung cấp dữ liệu xu hướng dài hạn hữu ích trong khoảng 12–24 tháng. Telomere ngắn có tương quan với bệnh tim mạch, suy giảm miễn dịch và tử vong sớm.
Điều này có ý nghĩa gì với bạn
Phối hợp các xét nghiệm này một cách chiến lược. Bạn không cần thực hiện tất cả mỗi quý.
- GlycanAge — Tốt nhất làm điểm kiểm tra sau 90 ngày khi thay đổi phác đồ
- Jinfiniti NAD+ — Xét nghiệm tại thời điểm ban đầu, sau đó lặp lại 60 ngày sau khi bắt đầu bổ sung NMN
- Xét nghiệm telomere — Một lần mỗi năm là đủ để thu được dữ liệu xu hướng có ý nghĩa
Tầng 3: Chỉ dấu sinh học máu tiêu chuẩn — La bàn hàng tháng của bạn
Đồng hồ sinh học chuyên sâu rất mạnh mẽ. Nhưng xét nghiệm máu tiêu chuẩn của bạn — khi được diễn giải qua lăng kính trường thọ — vẫn không thể thiếu.
Đây là các chỉ dấu mà bác sĩ chuyên khoa trường thọ của bạn cần theo dõi mỗi quý:
- hsCRP (protein C phản ứng siêu nhạy) — Chỉ dấu dễ tiếp cận nhất của tình trạng viêm hệ thống. Mức tối ưu cho trường thọ: dưới 0,5 mg/L (không phải mức “bình thường” thông thường dưới 3,0)
- IL-6 (Interleukin-6) — Một cytokine tiền viêm và là yếu tố thúc đẩy trực tiếp quá trình lão hóa do viêm (inflammaging). Mục tiêu: dưới 1,0 pg/mL
- Insulin lúc đói — Có giá trị dự đoán bệnh chuyển hóa cao hơn glucose đơn lẻ. Mức tối ưu: 2–5 μIU/mL
- IGF-1 (Yếu tố tăng trưởng giống Insulin 1) — Tín hiệu tăng trưởng và sửa chữa. Bạn cần giữ mức trung bình — không quá cao (nguy cơ ung thư) cũng không quá thấp (nguy cơ thiểu cơ). Khoảng tối ưu: 100–160 ng/mL tùy theo độ tuổi
- Homocysteine — Mức tăng cao báo hiệu rối loạn chức năng methyl hóa và nguy cơ tim mạch. Mục tiêu: dưới 7 μmol/L
- ApoB — Chỉ dấu dự đoán nguy cơ xơ vữa động mạch tốt nhất hiện có. Mức tối ưu cho trường thọ: dưới 60 mg/dL
💡 Kiến thức nhanh: Một phân tích tổng hợp năm 2022 trên Lancet cho thấy những người có hsCRP duy trì ổn định dưới 0,5 mg/L có nguy cơ tử vong do mọi nguyên nhân thấp hơn 44% so với những người trong khoảng “bình thường” 1,0–3,0 mg/L.
Điều này có ý nghĩa gì với bạn
Đừng chấp nhận các khoảng tham chiếu “bình thường”. Bình thường được xây dựng dựa trên một quần thể bệnh lý. Các khoảng tối ưu cho trường thọ chặt chẽ hơn đáng kể — và khoảng cách đó chính là nơi ẩn chứa hàng thập kỷ tuổi thọ khỏe mạnh.
- Yêu cầu thực hiện bộ xét nghiệm trường thọ đầy đủ mỗi 90 ngày trong năm đầu tiên
- Theo dõi xu hướng, không phải từng kết quả riêng lẻ — một lần đo đơn lẻ không có nhiều ý nghĩa; quỹ đạo mới là tất cả
- Kết hợp xét nghiệm máu với dữ liệu biểu sinh để có hồ sơ lão hóa đa chiều
Tầng 4: Dữ liệu từ thiết bị đeo — Vòng phản hồi sinh học hàng ngày
Xét nghiệm lâm sàng diễn ra mỗi quý. Cơ thể bạn gửi tín hiệu mỗi ngày.
- HRV (Biến thiên nhịp tim) — Đo bằng Oura Ring, WHOOP, hoặc Apple Watch, HRV phản ánh khả năng phục hồi của hệ thần kinh tự chủ. HRV cao hơn tương quan với tuổi sinh học thấp hơn, khả năng thích ứng stress tốt hơn và giảm tỷ lệ tử vong do tim mạch. Hãy theo dõi trung bình trượt 7 ngày, không phải các đỉnh dao động hàng ngày.
- Nhịp tim lúc nghỉ — Xu hướng nhịp tim lúc nghỉ giảm dần qua nhiều tháng báo hiệu hiệu quả tim mạch đang cải thiện. Mức tối ưu cho trường thọ: 50–60 nhịp/phút đối với hầu hết người trưởng thành.
- Cấu trúc giấc ngủ — Cụ thể là tỷ lệ giấc ngủ sâu và thời lượng giấc ngủ REM. Oura Ring cung cấp phân tích chi tiết nhất dành cho người dùng. Mục tiêu: 1,5–2 giờ giấc ngủ sâu, **1,5

Chân Trời 250 Năm: Tái Lập Trình Từng Phần Thay Đổi Tất Cả
Trong phần lớn lịch sử nhân loại, lão hóa là con đường một chiều.
Bạn sinh ra, bạn suy thoái, bạn chết đi. Câu hỏi duy nhất là quá trình ấy có “duyên dáng” đến đâu mà thôi. Câu chuyện đó đang đi đến hồi kết.
Một thế hệ khoa học mới — được rót hàng tỷ đô-la, được xác nhận bởi các đột phá tầm Nobel, và tăng tốc nhanh hơn bất kỳ lĩnh vực nào trong y sinh — đang viết lại những quy luật nền tảng. Không phải để làm chậm lão hóa. Mà để đảo ngược nó.
Cuộc Cách Mạng Yamanaka: Nút Khởi Động Lại Của Sinh Học
Vào năm 2006, nhà khoa học Nhật Bản Shinya Yamanaka phát hiện bốn gene — nay được gọi là các yếu tố Yamanaka (Oct4, Sox2, Klf4, c-Myc) — có khả năng tái lập trình một tế bào trưởng thành quay ngược về trạng thái tế bào gốc. Một tế bào da có thể trở nên trẻ lại. Đa tiềm năng. Nguyên sơ.
Ông nhận giải Nobel năm 2012. Nhưng trận địa chấn thực sự đến sau đó.
Các nhà nghiên cứu bắt đầu đặt ra một câu hỏi đột phá: nếu chỉ tái lập trình tế bào một phần thì sao? Không đưa ngược hoàn toàn về tế bào gốc — chỉ đủ xa để xóa sạch tổn thương biểu sinh do lão hóa, trong khi vẫn giữ nguyên bản sắc của tế bào.
Câu trả lời đã thay đổi tất cả:
- Các tế bào già phục hồi mô hình biểu hiện gene đặc trưng của tế bào trẻ — mà không mất chức năng
- Đồng hồ biểu sinh đảo ngược — các chỉ dấu tuổi sinh học quay ngược thời gian
- Chức năng mô được cải thiện — ở cơ, não, gan và mô mắt trên nhiều loài sinh vật khác nhau
💡 Quick Fact: Trong một nghiên cứu mang tính bước ngoặt tại Viện Salk năm 2016, tái lập trình từng phần đã kéo dài tuổi thọ ở chuột lão hóa sớm thêm 30% — và những con chuột này trông, vận động và lành vết thương như phiên bản trẻ hơn của chính chúng.
Đây không phải chống lão hóa. Đây là đảo ngược lão hóa.
Cuộc Đua Tỷ Đô Đã Bắt Đầu
Những nhà đầu tư và nhà khoa học hàng đầu thế giới không còn tranh luận liệu tái lập trình có hiệu quả hay không. Họ đang chạy đua để đưa công nghệ này đến con người.
Đây là những người dẫn đầu — và những gì họ đang xây dựng:
- Altos Labs (3 tỷ USD) — khoản đầu tư đơn lẻ lớn nhất trong lịch sử công nghệ sinh học, được tài trợ bởi Yuri Milner với sự tham gia của Jeff Bezos. Họ chiêu mộ chính Yamanaka, cùng các nhà khoa học đỉnh cao từ Stanford, Cambridge và Viện Salk. Sứ mệnh của họ: chuyển hóa tái lập trình từng phần thành y học lâm sàng.
- Retro Biosciences (180 triệu USD từ Sam Altman) — tập trung vào tái lập trình tế bào, tự thực bào (autophagy) và các liệu pháp lấy cảm hứng từ huyết tương. Mục tiêu công bố: cộng thêm 10 năm khỏe mạnh vào tuổi thọ con người — chỉ là điểm khởi đầu.
- Phòng thí nghiệm của GS. David Sinclair tại Harvard — đã chứng minh rằng liệu pháp gene OSK (ba trong bốn yếu tố Yamanaka) phục hồi thị lực ở chuột mù bằng cách đưa tế bào hạch võng mạc về trạng thái biểu sinh trẻ hơn. Công bố trên Nature (2020). Nhóm nghiên cứu của ông sau đó đã chứng minh khả năng đảo ngược tuổi sinh học ở nhiều loại mô khác nhau.
- Turn Biotechnologies — đang phát triển công nghệ tái lập trình từng phần dựa trên mRNA, có thể được đưa vào cơ thể theo dạng nhất thời, tránh nguy cơ hình thành khối u. Dữ liệu ban đầu cho thấy đảo ngược tuổi biểu sinh ở tế bào da và cơ người lên đến 20 năm.
- Chương trình Blueprint của Bryan Johnson — chi 2 triệu USD mỗi năm cho phác đồ trường thọ tích cực nhất từng được ghi nhận, đo lường mọi hệ cơ quan hàng tháng, và công khai chứng minh rằng tuổi sinh học có thể lệch xa đáng kể so với tuổi lịch. Tốc độ lão hóa biểu sinh của ông: 0,69 (lão hóa chỉ bằng 69% tốc độ bình thường).
Bạn rất có thể sẽ tiếp cận được một dạng liệu pháp tái lập trình nào đó trong vòng 10–20 năm tới. Liệu pháp gene. Phương pháp điều trị bằng mRNA. Các phân tử nhỏ mô phỏng tác dụng của các yếu tố Yamanaka mà không cần biến đổi di truyền.
Nhưng đây là điều hầu hết mọi người bỏ qua:
Hiệu quả của tái lập trình tỷ lệ thuận với tình trạng của cơ thể tiếp nhận nó.
Một hệ biểu sinh khỏe mạnh hơn hôm nay đồng nghĩa với đáp ứng tái lập trình tốt hơn ngày mai. Mỗi phác đồ trong bộ hướng dẫn này — mỗi mục tiêu viêm được xử lý, mỗi mức NAD+ được tối ưu hóa, mỗi chỉ số chuyển hóa được đưa về vùng trường thọ — đều đang chuẩn bị bộ máy tế bào của bạn cho những liệu pháp mạnh mẽ nhất trong lịch sử y học nhân loại.
Đây là chiến lược cầu nối:
- Tối ưu hóa ngay bây giờ — để tuổi sinh học của bạn trẻ hơn tuổi lịch 10–20 năm
- Theo dõi không ngừng — bằng đồng hồ biểu sinh, bảng xét nghiệm viêm và các chỉ dấu sinh học chuyển hóa
- Đến đích trong tình trạng tốt nhất có thể khi tái lập trình, liệu pháp thanh thải tế bào lão hóa (senolytics), và tái tạo cơ quan đạt mức sẵn sàng lâm sàng
Tuổi Thọ Khỏe Mạnh Chính Là Tuổi Thọ — Đó Là Chuẩn Mực Mới
Mục tiêu chưa bao giờ chỉ là thêm năm tháng. Mà là thêm sức sống cho mỗi năm.
Khoa học hiện đang hội tụ — từ tái lập trình từng phần, đến khám phá thuốc bằng AI, đến y học biểu sinh cá thể hóa — đều hướng đến một tương lai nơi 150 tuổi không phải viễn tưởng, và 250 tuổi là một bài toán kỹ thuật chính đáng. Không phải phép màu. Là bài toán. Và bài toán thì có lời giải.
Những gì bạn làm hôm nay không tách rời khỏi tương lai ấy. Nó chính là nền móng của tương lai ấy.
Điểm Mấu Chốt
- Tái lập trình từng phần đã đảo ngược tuổi sinh học trong mô động vật — phục hồi thị lực, chức năng cơ và trạng thái biểu sinh trẻ trung mà không mất bản sắc tế bào
- Altos Labs, Retro Biosciences và phòng thí nghiệm Sinclair tại Harvard đang dẫn đầu cuộc đua trị giá hàng tỷ đô-la nhằm đưa liệu pháp tái lập trình đến con người trong thập kỷ tới
- Phác đồ trường thọ của bạn hôm nay chính là cây cầu dẫn đến ngày mai — hệ biểu sinh của bạn càng khỏe mạnh khi các liệu pháp này ra đời, hiệu quả bạn nhận được sẽ càng vượt trội
Câu Hỏi Thường Gặp
Có — và bằng chứng nay đã vượt ra ngoài tranh luận. Nhiều thử nghiệm lâm sàng được đánh giá đồng nghiệp ghi nhận sự đảo ngược có thể đo lường được. Thử nghiệm senolytic dasatinib+quercetin của Mayo Clinic cải thiện chức năng thể chất, tốc độ đi bộ và sức mạnh nắm tay ở bệnh nhân cao tuổi. Lab Sinclair của Harvard phục hồi thị lực ở chuột già qua tái lập trình biểu sinh (các yếu tố OSK). Đồng hồ biểu sinh Horvath — chỉ dấu lão hóa được xác nhận nhất — cho thấy đảo ngược tuổi sinh học 2–8 năm trong các nghiên cứu can thiệp lối sống có kiểm soát. Thông điệp cốt lõi: lão hóa là vấn đề thông tin, không phải entropy. Bộ gen giữ nguyên bản thiết kế trẻ trung; nó chỉ cần tín hiệu đúng để biểu hiện lại.
Tài Liệu Tham Khảo
- Baker DJ et al. “Clearance of p16Ink4a-positive senescent cells delays ageing-associated disorders.” Nature, 2011. ↗
- Igarashi M et al. “Chronic nicotinamide mononucleotide supplementation elevates blood NAD levels in healthy subjects.” npj Aging, 2022. ↗
- Sinclair DA & Guarente L “Unlocking the secrets of longevity genes.” Scientific American, 2006. ↗
- Kirkland JL et al. “The clinical potential of senolytic drugs.” Journal of the American Geriatrics Society, 2017. ↗
- Zou Y et al. “Fisetin is a senotherapeutic that extends health and lifespan.” EBioMedicine, 2018. ↗
- Yoshino J et al. “Nicotinamide mononucleotide treats the pathophysiology of diet- and age-induced diabetes in mice.” Cell Metabolism, 2011. ↗
- López-Otín C et al. “Hallmarks of aging: An expanding universe.” Cell, 2023. ↗
- Eisenberg T et al. “Cardioprotection and lifespan extension by the natural polyamine spermidine.” Nature Medicine, 2016. ↗




Leave A Comment